Лечение ОРДС. Часть 2
Во время проведения искусственной вентиляции легких при ОРДС для принятия решения о...
Специалистам / Протоколы лечения / Протоколы лечения (статья)
 ОРДСИНТЕНСИВНАЯ ТЕРАПИЯ
ОРДСИНТЕНСИВНАЯ ТЕРАПИЯОптимальная тактика интенсивной терапии при остром респираторном дистресс-синдроме (ОРДС) подразумевает дифференцированный подход в зависимости от этиологического фактора, длительности и основных патогенетических механизмов (см статью «Острый Респираторный Дистресс-Синдром: Общие сведения для врачей»).
Клиническое течение ОРДС, ответ на лечение (в том числе ответ на респираторную поддержку и рекрутирование альвеол) и другие особенности зависят от основной патологии, причины развития, типа и патоморфологических особенностей синдрома.
Принципы интенсивной терапии (ИТ) в значительной степени зависят от этиологии, патогенетического фактора и тяжести течения острого респираторного дистресс-синдрома. При этом основными целями ИТ являются:
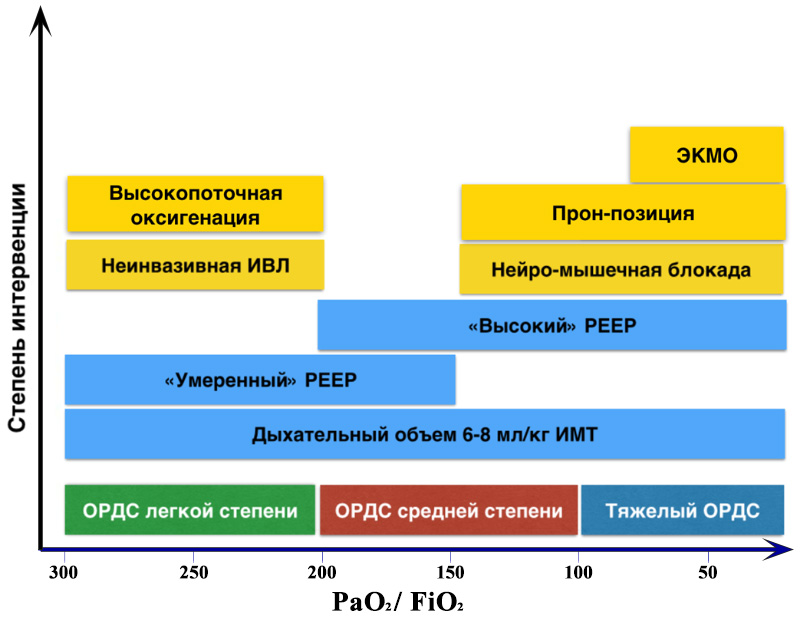
Степень интервенции при остром респираторном дистресс-синдроме. Схема пошагового подхода к терапии острого респираторного дистресс-синдрома, основанная на данных мультицентровых рандомизированных контролируемых исследований
Разные режимы респираторной поддержки являются методом временного протезирования функции внешнего дыхания, что позволяет обеспечить поддержку газообмена в легких, снижает работу дыхания и дает возможность восстановить легочную функцию. В некоторых случаях при ОРДС можно поддержать адекватный газообмен в легких при спонтанном дыхании с помощью ингаляции кислорода и PEEP (положительным конечно-экспираторным давлением), или с помощью применения неинвазивных методов респираторной поддержки. Тем не менее, некоторые мультицентровые когортные исследования показывают, что в большинстве случаев при ОРДС (до 85%) необходимо проводить инвазивную вспомогательную или полностью контролируемую ИВЛ.
Интубация трахеи и инвазивная искусственная вентиляция легких при ОРДС показана в следующих случаях:
С точки зрения физиологии и элементарной логики эндотрахеальную интубацию следует проводить при полном отсутствии дыхания (апноэ, остановка кровообращения), также интубация трахеи показана при высоком риске аспирации (делирий, нарушение сознания) и нарушении функции голосовых складок. По этическим соображениям рандомизированные контролируемые исследования по оценке абсолютных показаний для искусственной вентиляции легких не проводились.
В большинстве случаев при ОРДС абсолютные показания к эндорахеальной интубации (нарушение глоточных рефлексов, нарушение сознания, парез голосовых складок) обусловлены другими причинами – травма, шок, сепсис, полинейропатия критических состояний, полиорганная недостаточность.
Исследования по относительным и абсолютным показаниям к проведению респираторной поддержки по этическим соображениям не проводились. Представленные показания основаны на разработках экспертного консенсуса, опубликованных в 1993 году (с тех пор они не изменялись):
В крупном мультицентровом когортном исследовании интубировали и подключили к ИВЛ 85% больных с ОРДС (большинство – в первые 24 часа с момента появления первых признаков ОРДС). Перед интубацией средний показатель PaO2/FiO2 у этих пациентов составлял 146±84 мм рт ст, в 74% случаев у больных был шок или необходимость в катехоламиновой поддержке (другие факторы были не столь важными).
В другом аналогичном исследовании при ОРДС изначально интубировали 70% больных. У 30% больных применялась неинвазивная искусственная вентиляция легких, в 46% из которых она не дала ожидаемого результата. В итоге частота проведения инвазивной ИВЛ в общем составила 84%.
Высокопоточная назальная оксигенация (в отличие от кислородных назальных масок или обыкновенной кислородной маски) позволяет обеспечить поток кислорода до 60 л/мин, что максимально соответствует к показателю величины пикового инспираторного потока (стандартная оксигенотерапия обеспечивает поток кислорода в объеме до 15 л/мин, а инспираторную фракцию кислорода не более 35%).
Исследования показали отсутствие десатурации при эндотрахеальной интубации при тяжелом и среднетяжелом течении ОРДС при использовании высокопоточной оксигенации до и во время интубации, в отличие от использования лицевой маски с мешком (при этом у 14% больных отмечалось SpO2 < 80%).
Другое исследование, где сравнивали эффект от высокопоточной назальной оксигенации с эффектом от вентиляции через маску и мешок у больных с умеренной гипоксемией (средний показатель PaO2/FiO2 составлял 200 мм рт ст), показало отсутствие разницы по частоте десатурации во время интубации. Тем не менее, при длительной интубации в группе с маской и мешком наблюдалось снижение SpO2.
Исследования показали, что поздняя интубация (на 2-4 день с момента развития ОРДС) приводит к повышению показателя летальности с 36% до 56%.
В соответствии с кривой насыщения гемоглобина и формулы доставки кислорода, повышение показателя SpO2 > 90% приводит к незначительному повышению доставки кислорода. Учитывая это, в международных клинических рекомендациях целевой показатель уровня оксигенации SpO2 – 88-95%, PaO2 – 55-80 мм рт ст.
Повышение целевых значения PaCO2 допускается при хронической гиперкапнии (обусловленной, например, ХОБЛ), тяжелом течении ОРДС, отсутствии патологии головного мозга. В таких случаях целевое значение либо не удается достичь, либо для его достижения нужно нарушать протокол «протективной» вентиляции легких. При этом допускается применение методологии «допустимой гиперкапнии» с поддержкой уровня PaCO2 не превышает показатель 60 мм рт ст.
Дыхательный объем – интеграл потока по времени (общая сумма доставленного потока во время вдоха). Поступление дыхательного объема осуществляется за счет нескольких типов профиля потока. Так, в аппаратах искусственной вентиляции легких I-го поколения в качестве генератора потока применяли мех, что вызывало генерацию потока постоянной (прямоугольной) формы. Эти режимы получили название «режимы с управляемым объемом» (volume-controlled ventilation), поскольку дыхательный объем зависел от объема меха, который устанавливал врач. Прямоугольная форма инспираторного потока характеризуется постоянным увеличением давления при вдохе, возникновением пикового давления в дыхательных путях (без поддержания постоянного давления в дыхательных путях – давление плато).
Создание микропроцессорных аппаратов искусственного дыхания позволило создавать профиль потока максимально соответствующего профилю потока у здорового человека (нисходящий поток). Нисходящий поток характеризуется быстрым увеличением давления в дыхательных путях и его удержанием (создаваемое инспираторное давление аналогично давлению плато), что получило название «вентиляция с управляемым давлением» (pressure-controlled ventilation или pressure support ventilation). Современные аппараты ИВЛ в режимах VC (управляемым объемом) используют нисходящий профиль потока. То есть, дыхательный объем задает врач, а аппарат производит расчет инспираторного давления с учетом податливости респираторной системы больного. Таким образом, при использовании нисходящего профиля потока в современных аппаратах искусственной вентиляции легких нет разницы между режимами PC и VC.
Нисходящий профиль потока позволяет обеспечить максимально равномерное распределение объема газа между участками легких с разной постоянной времени, что является более физиологичным при остром респираторном дистресс-синдроме, а также создает меньшее давление в дыхательных путях.
Некоторые клиницисты полагают, что при ОРДС целесообразно использовать вентиляцию с тремя уровнями давления, таким образом оптимизируется распределение газа в легких.
Режимы полностью вспомогательной вентиляции легких включают:
Режимы с заданными врачом аппаратными вдохами относят:
Отметим, что при управляемой искусственной вентиляции легких газ в основном распределяется по вышележащим отделам легких, а в нижних и наддиафрагмальных отделах возникают ателектазы (см статью «Рентгенография: Ателектаз»), что вызывает нарушение вентиляционно-перфузионного отношения, прогрессирование гипоксемии, а также может привести к возникновению вентилятор-ассоциированной пневмонии.
Во время управляемой ИВЛ диафрагма не задействована в процессе дыхания, что вызывает ее атрофию, которая у критических больных подвержена выраженному катаболизму. Исследования показывают, что использование управляемой ИВЛ увеличивает десинхронизацию больного с респиратором, в результате увеличивается срок респираторной поддержки и ухудшается прогноз.
Эксперимент, проведенный у больных с легким с среднетяжелым ОРДС, продемонстрировал улучшение оксигенации, распределение газа и гистологических показателей на фоне полностью вспомогательной ИВЛ. То есть, в случае применения управляемых режимов респираторной поддержки при легком и среднем течении ОРДС рекомендуется как можно быстрее переходить на режимы вспомогательной вентиляции.
PSV (Pressure Support Ventilation) является основой всех вспомогательных режимов респираторной поддержки. Современные варианты PSV (например, PAV+) способствуют лучшей синхронизации больного с вентилятором и снижают работу дыхания больного.
Неинвазивная искусственная вентиляция легких позволяет избежать эндотрахеальной интубации у больных с легким и умеренным течением ОРДС. Успешное применение неинвазивной респираторной поддержки позволяет снизить частоту нозокомиальной пневмонии и смертности. Оценка клинической эффективности НИВЛ при остром респираторном дистресс-синдроме проводится через 1 час после начала процедуры: если у больного отмечается снижение показателя PaO2/FiO2 < 175 мм рт ст, десинхронизация с респиратором, повышение ЧД > 25-30 в минуту, повышение показателя PaCO2, развитие ацидоза, необходимо проводить эндотрахеальную интубация и инвазивную ИВЛ.
В случае неэффективности НИВЛ (гипоксемия, метаболический ацидоз, индекс PaO2/FiO2 не повышается более 175 мм рт ст в течение 2 часов, повышенной работе дыхания [десинхронизация с респиратором, в процессе дыхания участвует вспомогательная мускулатура, «провалы» при триггировании вдоха на кривой «давление-время]), больного нужно интубировать. При отсутствии эффективности неинвазивной ИВЛ задержка эндотрахеальной интубации ухудшает прогноз и повышает показатель смертности.
Показатель дыхательного объема у здорового человека составляет примерно 6 мл/кг ИМТ. Расчет ИМТ проводится по следующим формулам:
Мужчины: ИМТ (кг) = 50 + 0,91 (Рост [см] – 152,4)
Женщины: ИМТ (кг) = 45,5 + 0,91 (Рост [см] – 152,4)
Исследования показали, что при сравнительно равных показателях PEEP и autoPEEP из-за инверсного соотношения вдоха к выдоху (более 1:1,2), инверсия вызывает большее нарушение распределения локальных конечно-экспираторных давлений и конечно-экспираторных объемов, что непрогнозируемо влияет на изменение конечно-экспираторных давления и объемов, а также за счет давления на легочные капилляры вызывает повышение постнагрузки правого желудочка. Таким образом, при адекватной настройке PEEP и использовании маневров рекрутирования, соответствующих показаниям, преимущества перед autoPEEP при применении инверсного соотношения вдоха к выдоху отсутствуют.
Чтобы предотвратить инверсное соотношение вдоха к выдоху, нужно установить Tinsp (инспираторное время, время вдоха) в пределах 0,8-1,2 секунды за счет установки параметра вдоха или регуляции скорости потока (чем больше скорость потока, тем короче время вдоха). Диапазон регуляции скорости потока – 40-80 л/мин.
В качестве метода резерва в рамках режима APRV (вентиляция легких со сбросом давления) можно применять инвертированное соотношение вдоха к выдоху.
Исследования показали, что вспомогательные режимы респираторной поддержки обладают преимуществом перед режимами ИВЛ с заданными аппаратными вдохами.
Разные варианты вспомогательных режимов современных аппаратов искусственной вентиляции легких (например, PAV+, ASV, PPS, iSV и др) широко не распространены, поэтому описание настроек ИВЛ для этих режимов в данной статье не рассмотрены.
Чтобы улучшить синхронизацию больного с вентилятором в режиме PS, применяют несколько способов:
При этом необходимо изначально снизить избыточное PS и оценить критерии готовности к отлучению, а при достижении целевых параметров, провести тест спонтанного дыхания.
Настройка инспираторного триггера имеет небольшое значение в общей работе дыхания и десинхронизации больного с вентилятором. Отметим, что аппараты ИВЛ, произведенные до 2000 года, имеют триггеры более низкого качества, чем в более новых аппаратах, поэтому преимущество имели триггеры потока. Современные аппараты ИВЛ переход с триггера давления на триггер потока, как правило, качество триггирования не улучшает.
Уменьшение работы дыхания характеризуется показателем значения работы дыхания в пределах 0,25-0,5 Дж/л (при доступном мониторинге функции дыхания). Если больной находится на вспомогательных режимах ИВЛ и/или нет возможности контролировать функцию дыхания, в качестве критерия оценки используют соотношение ЧД к ДО (индекс Тобина), показатель которого при условии нормального дыхания больного не превышает 70.
Если на фоне достижения целевых значений ЧД, ДО и показателей газообмена больной чувствует дискомфорт, необходимо предпринять следующие действия:
В случае нарушения нейромышечной проводимости или центральной регуляции дыхания (апноэ, гиперпноэ, патологические ритмы дыхания), использование установленного аппаратом дыхательного ритма позволяет предупредить развитие гипоксемии и гиперкапнии.
ПРОДОЛЖЕНИЕ ЗДЕСЬ: «Лечение ОРДС. Часть 2»
Во время проведения искусственной вентиляции легких при ОРДС для принятия решения о...
При ОРДС с индексом PaO2 / FiO2 < 150 мм рт ст при PEEP > 8 мбар (особенно при первичном...
Рекомендации по формированию клинического диагноза распространяются на все состояния и...
Острый респираторный дистресс-синдром (ОРДС; МКБ-10: J80 – Синдром респираторного...
Даже при условии усиленной подачи кислорода (10-15 л/мин) через маску с резервуаром и высоким...
анализы, БАД, биологическая медицина, витамины, гастроэнтерология, гигиена, гинекология, гомеопатия, дерматология, диагностика, диетология, заболевания, иммунология, инфекционные заболевания, инфекция, исследования, кардиология, кожа, косметика, красота, лекарственные растения, лечение, лицо, неврология, обследование, оздоровление, онкология, ортопедия, педиатрия, питание, пищеварительная система, поведение, похудение, препараты, продукты, профилактика, процедура, психология, пульмонология, рак, реабилитация, сердечно-сосудистая система, ССС, тело, терапия, травматология, уход, фитотерапия, хирургия, эндокринология
Показать все теги

Комменатрии к новости