Диагностика боли в грудной клетке
Довольно часто на амбулаторном приеме к семейному врачу или врачу-терапевту обращаются...
Медицина / Патология / Патология (статья)
 Легочная гипертензияСогласно определению Европейского общества кардиологов — ЕОК (2008 г.), легочная гипертензия (ЛГ) — это гемодинамическое и патофизиологическое состояние, характеризующееся повышением давления в легочной артерии (ЛА) до 25 мм рт. ст. и выше, которое определяют по данным катетеризации правых отделов сердца.
Легочная гипертензияСогласно определению Европейского общества кардиологов — ЕОК (2008 г.), легочная гипертензия (ЛГ) — это гемодинамическое и патофизиологическое состояние, характеризующееся повышением давления в легочной артерии (ЛА) до 25 мм рт. ст. и выше, которое определяют по данным катетеризации правых отделов сердца.
Основы изучения параметров гемодинамики малого круга кровообращения и изменений давления в легочной артерии заложил W. Forssmann, который доказал безопасность катетеризации правых отделов сердца. Дальнейшее внедрение этого метода в клиническую практику A. Cournand и D. Richard получило признание научной общественности и было удостоено Нобелевской премии в области медицины. В настоящее время методы катетеризации камер сердца и сосудов совершенствуются, что способствует их широкому внедрению в клиническую практику.
Повышение давления в легочной артерии — синдром, который выявляют при различных заболеваниях.
В зависимости от локализации повышенного сопротивления в сосудах легких (ЛСС) различают следующие формы легочной гипертензии:
Наиболее распространенной является Клиническая классификация легочной гипертензии, предложенная в 1998 г. и пересмотренная впоследствии экспертными комиссиями в Венеции (2003 г.) и Калифорнии (2008 г.) (см. табл.).
|
1. Легочная артериальная гипертензия (ЛАГ) |
|
|
1.1 Идиопатическая легочная гипертензия (ИЛГ) |
|
|
1.2 Наследственная |
1.2.1 Bone morphogenetic protein receptor 2 — BMRP2 |
|
1.2.2 Activin receptor-like kinase 1-gene — ALK1, endolgin (с врожденной геморрагической телеангиэктазией или без нее) |
|
|
1.2.3 Неизвестной этиологии |
|
|
1.3 Ассоциированная с действием лекарств или токсинов |
|
|
1.4 Ассоциированная со следующими состояниями: |
1.4.1 Ревматическими заболеваниями |
|
1.4.2 ВИЧ-инфекцией |
|
|
1.4.3 Портальной гипертензией |
|
|
1.4.4 Врожденными пороками сердца |
|
|
1.4.5 Шистосомозом |
|
|
1.4.6 Хронической гемолитической анемией |
|
|
1.5 Персистирующая легочная гипертензия новорожденных |
|
|
1.6 Веноокклюзионная болезнь легких и/или гемангиоматоз легочных каппиляров |
|
|
2. Легочная гипертензия, ассоциированная с поражением левой половины сердца |
2.1 Систолическая дисфункция |
|
2.2 Диастолическая дисфункция |
|
|
2.3 Заболевания клапанов сердца |
|
|
3. Легочная гипертензия, ассоциированная с заболеваниями легких и/или гипоксией |
3.1 При ХОЗЛ |
|
3.2 При интерстициальных болезнях легких |
|
|
3.3 При других заболеваниях легких со смешанными обструктивно-рестриктивными причинами |
|
|
3.4 Легочная гипертензия при нарушениях сна |
|
|
3.5 Легочная гипертензия при гиповентиляционной патологии альвеол |
|
|
3.6 Легочная гипертензия при длительном пребывании в условиях высокогорья |
|
|
3.7 Легочная гипертензия при пороках развития легких |
|
|
4. Хроническая посттромбоэмболическая легочная гипертензия |
|
|
5. Легочная гипертензия с неизвестными и/или многофакторными механизмами |
5.1 Гематологические заболевания: миелопролиферативные заболевания, состояние после спленэктомии |
|
5.2 Системные заболевания, саркоидоз, гистоцитоз Х, лимфангиолейомиоматоз, нейрофиброматоз, васкулит |
|
|
5.3 Метаболические нарушения: болезни накопления гликогена, болезнь Гоше, заболевания щитовидой железы |
|
|
5.4 Другие причины: опухолевая обструкция, фиброзирующий медиастинит, хроническая почечная недостаточность при пребывании на диализе |
|
В настоящее время особое внимание экспертов привлечено к легочной артериальной гипертензии, так как именно эта форма легочной гипертензии характеризуется наиболее серьезным прогнозом. Разработка современных видов лечения также ориентирована на пациентов данной группы.
Для оценки выраженности легочной гипертензии используют рекомендации ВОЗ (2003 г.) с выделением 3 степеней повышения давления в легочной артерии:
- легкая (25-45 мм рт. ст.);
- средняя (46-65 мм рт. ст.);
- выраженная (выше 65 мм рт. ст.).
Эксперты ВОЗ (1998 г.) предложили определять функциональный класс (ФК) сердечной недостаточности (СН) у больных с легочной гипертензией, что позволит установить тяжесть и прогноз при ЛГ, а также уточнить показания к проведению различных методов лечения и оценить их эффективность:
I ФК — отсутствие значимого ограничения физической активности, обычная активность не вызывает увеличения выраженности одышки, слабости, боли в груди, пресинкопе (бессимптомная легочная гипертензия);
II ФК — умеренное снижение физической активности; отсутствие дискомфорта в покое, но обычный уровень активности вызывает появление умеренно выраженных симптомов (одышки, слабости, боли в груди, пресинкопе);
III ФК — значительное снижение физической активности. Отсутствие дискомфорта в покое, но уровень активности ниже обычного вызывает появление умеренно выраженных симптомов (одышки, слабости, боли в груди, пресинкопе);
IV ФК — одышка и/или слабость в покое. Выраженность симптомов увеличивается при минимальной нагрузке. Неспособность выполнять любую физическую нагрузку, возможны признаки правожелудочковой недостаточности.
Принято считать, что легочная гипертензия является достаточно распространенным заболеванием, хотя истинная заболеваемость и смертность от этой патологии (преимущественно легочная артериальная гипертензия) изучены недостаточно, а имеющиеся сведения базируются на данных национальных центров по изучению этого синдрома и результатах научных исследований. В соответствии с данными национального французского регистра распространенность легочной артериальной гипертензии составляет 15 случаев на 1 млн человек и почти в половине случаев (6 на 1 млн человек) представлена идеопатической легочной гипертензией. Признаки ЛГ выявляют у 80% пациентов с ревматическими заболеваниями, в 6 раз чаще при портальной гипертензии и в 6-12 раз чаще у инфицированных вирусом иммунодефицита человека (ВИЧ), чем в общей популяции.
Для всех форм легочной гипертензии общими признаками являются гипертрофия и/или дилатация правого желудочка (ПЖ) сердца, расширение основного ствола и основных ветвей легочной артерии. Интима этих сосудов имеет несколько эластических мембран, придающих ей слоистое строение (рис. 1). При развитии легочной гипертензии стенки ствола и крупных ветвей утолщаются, отмечается липоидоз их стенок. Выраженность этих изменений зависит от степени повышения давления в легочной артерии, величины и локализации сопротивления сосудов легких, а также от длительности заболевания.
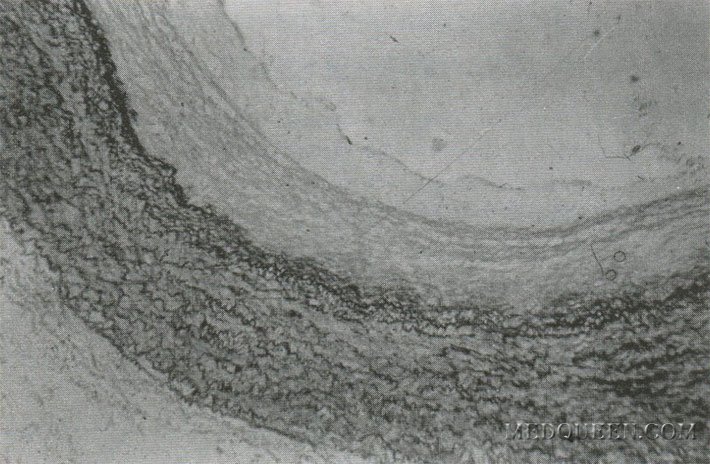
Рис. 1. Стенка крупного ствола ЛА. Слоистое строение интимы
У больных с прекапиллярной формой легочной гипертензии изменения в сосудах системы легочной артерии значительно выражены и отмечаются во всех слоях стенки с пролиферацией интимы вплоть до облитерации сосуда (рис. 2), развития внутрилегочных шунтов и образования гломусных анастомозов (рис. 3). Часто обнаруживают микротромбозы. В легочных венах мышечный слой, как правило, атрофирован.
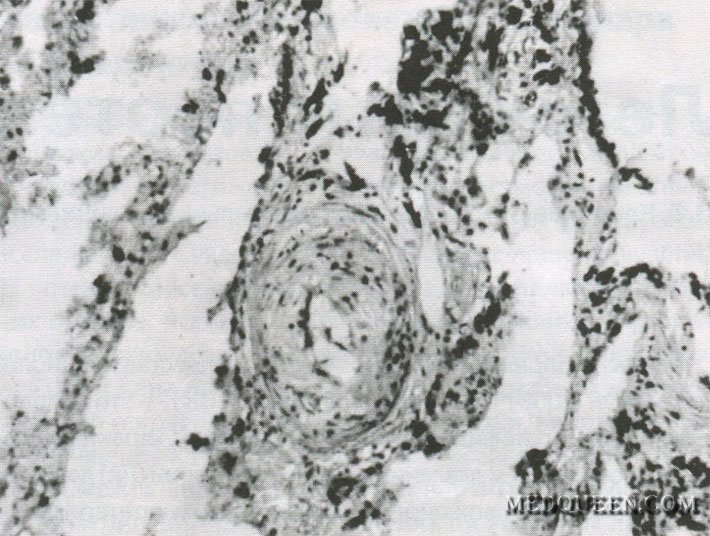
Рис. 2. Пролиферация интимы в мелком легочном сосуде
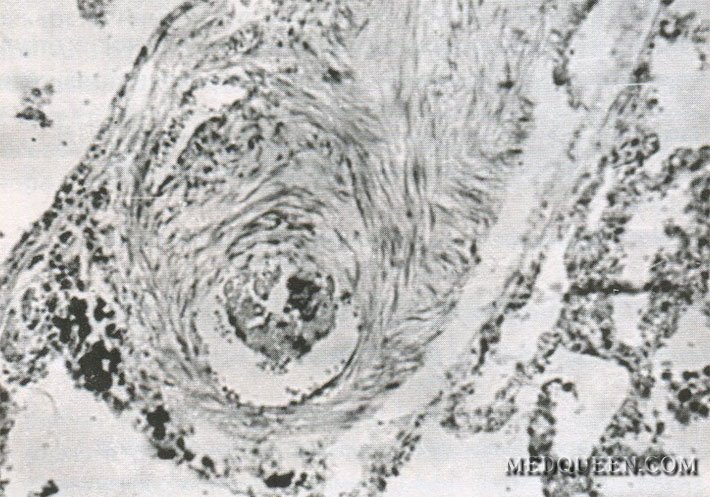
Рис. 3. Гломусный анастомоз
При посткапиллярной легочной гипертензии в артериолах и мелких артериях выражена гипертрофия циркулярных мышечных волокон, появляются дополнительные эластические мембраны и продольный мышечный слой, расположенный медиально от внутренней эластической мембраны. Характерны выраженная гипертрофия мышечных элементов мелких вен и склероз их интимы.
Патогенетические механизмы легочной гипертензии разнообразны, причем в ее возникновении и прогрессировании при различных заболеваниях могут принимать участие несколько патогенетических факторов одновременно или последовательно. В свете новых представлений ключевым звеном патогенеза легочной гипертензии признана эндотелиальная дисфункция (ЭД) легочных сосудов. Она может возникнуть в результате наследственных механизмов, под влиянием факторов внешней среды, которые изменяют баланс метаболизма оксида азота (NО), с одной стороны, и эндотелина и тромбоксана — с другой. Это приводит к нарушениям вазоактивности легочных сосудов и их вазоконстрикции. Еще одним важным компонентом патогенеза легочной гипертензии является снижение синтеза простациклина, вследствие чего активируются внутриклеточные механизмы, запускающие гиперплазию и гипертрофию гладкомышечных элементов, апоптоз, пролиферацию, фибробластоз, воспаление и ангиогенез.
Одними из ключевых моментов в развитии легочной гипертензии являются повышение концентрации эндотелина и активация рецепторов к нему. Причиной этого может быть как увеличение его продукции, так и уменьшение утилизации в легких. Эффекты эндотелина реализуются посредством эндотелиновых рецепторов А- и В-типов. А-рецепторы находятся на гладких мышечных клетках, а В-рецепторы — на клетках эндотелия. Другими важными механизмами в патогенезе легочной гипертензии являются нарушение синтеза или доступности NО и активация тромбоцитов, которая сопровождается высвобождением целого ряда биологически активных веществ: серотонина, факторов свертываемости крови, тромбоцитарного фактора роста, вследствие чего в системе легочной артерии развивается прокоагулянтное состояние и возникают тромботические осложнения, которые приводят к основным эффектам эндотелиальной дисфункции, характерным для всех форм легочной артериальной гипертензии (рис. 4):
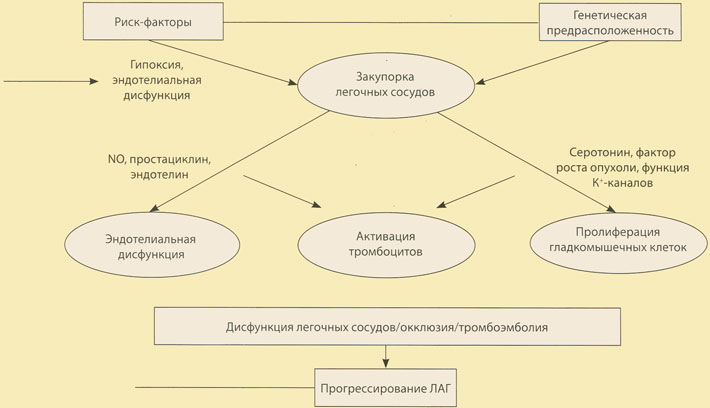
Рис. 4. Алгоритм патофизиологических изменений при ЛАГ
Венозная (посткапиллярная) легочная гипертензия. К эндотелиальной дисфункции легочных сосудов более чем в 80-90% случаев приводит поражение левых отделов сердца, сопровождающееся повышением давления в левом предсердии. При митральной недостаточности, аортальных пороках, ишемической болезни сердца (ИБС) и дилатационной кардиомиопатии (ДКМП) основной причиной повышения давления в левом предсердии является нарушение систолической функции левого желудочка (ЛЖ) сердца, а при артериальной гипертензии, гипертрофической кардиомиопатии (ГКМП) и амилоидозе сердца систолической дисфункции предшествует диастолическая дисфункция. При митральном стенозе, миксоме левого предсердия и его тромбозе, в том числе шаровидном, давление в левом предсердии повышается из-за нарушения оттока крови из него.
У больных с перечисленной патологией систолическое давление в легочной артерии (СДЛА), как правило, не достигает высоких цифр и соответствует I-II степени легочной гипертензии. Исключением является митральный стеноз, при котором возможно его повышение до 100 мм рт. ст. и выше, нормализующееся, как правило, через 6-12 мес после комиссуротомии или баллонной вальвулотомии.
Легочно-артериальная (прекапиллярная) гипертензия неоднородна по патогенезу.
При тромбоэмболии легочной артерии (ТЭЛА) легочная гипертензия развивается по двум основным механизмам:
При ревматических заболеваниях соединительной ткани (системная склеродермия, системная красная волчанка, полиартериит, аорто-артериит с поражением системы ЛА и др.) пусковым механизмом в патогенезе легочной гипертензии является уменьшение сосудистого русла легочной артерии и повышение ЛСС за счет воспалительных и склеротических изменений в этих сосудах, приводящих к ЭД сосудов.
В основе повышения СДЛА у пациентов с ХОЗЛ и при торакодиафрагмальных болезнях, ночном апноэ, синдроме Пикквика, а также улиц, проживающих в условиях высокогорья, основной причиной ЭД легочных сосудов является альвеолярная гипоксия, что было доказано в классических работах Эйлера и Лильестранда (1946) и известно как рефлекс Эйлера-Лильестранда. Механизмы спазма легочных сосудов при альвеолярной гипоксии до настоящего времени полностью не раскрыты. Согласно имеющимся данным, медиаторами сужения сосудов являются катехоламины, гистамин, ангиотензин II, тромбоксан А2 и некоторые другие простагландины, вазопрессин и некоторые лейкотриены. Следует отметить, что вазоактивные медиаторы регулируют не только сосудистый тонус, но и проницаемость сосудистой стенки, влияют на тромбообразование и пролиферацию гладкомышечных клеток сосудистой стенки и фибробластов. Зачастую эти изменения носят локальный характер соответственно участкам гиповентиляции альвеолярной ткани.
К патогенетическим механизмам легочной гипертензии у пациентов с ХОЗЛ относятся также нарушение функции дыхательных мышц, повышение внутригрудного давления, увеличение минутного объема крови в результате гипоксического раздражения хеморецепторов аортальной и синокаротидной зоны, нарушение реологии крови с формированием вторичной полицитемии. При развитии легочной гипертензии у больных с ночным апноэ имеет значение частичное сужение верхних дыхательных путей во время сна.
По результатам многочисленных клинических исследований с выполнением катетеризации правого желудочка и легочной артерии, проведенных с участием этих больных, сделан важный вывод о том, что СДЛА при бронхолегочных заболеваниях, как правило, достигает не более 40-50 мм рт. ст., прогрессирует крайне медленно, возрастая за 2-3 года в среднем на 2 мм рт. ст., либо практически не изменяется. В то же время следует заметить, что даже небольшое повышение давления в легочной артери у таких больных может иметь прогностическое значение. При СДЛА >45 мм рт. ст. продолжительность жизни редко превышает 5 лет.
При врожденных пороках сердца (ВПС) с увеличенным легочным кровотоком: дефекте межжелудочковой перегородки (ДМЖП), открытом артериальном протоке (ОАП), дефекте межпредсердной перегородки (ДМПП) — различают врожденную и приобретенную формы легочной гипертензии. Впервые мнение о врожденном характере легочной гиперензии при этих пороках высказал Edwards (1950), который обнаружил сходство в строении легочных сосудов у плода и умерших больных с комплексом Эйзенменгера. В этих случаях уже в раннем детском возрасте у больных с ВПС доминируют признаки ЛГ с высоким ЛСС, на фоне которого артериовенозный сброс практически отсутствует или возникает обратный сброс крови. Эту форму легочной гипертензии при врожденных пороках сердца некоторые авторы называют «врожденным комплексом Эйзенменгера». Однако при ВПС чаще наблюдают приобретенную форму ЛГ, патогенез которой связан с гиперволемией малого круга, которая вначале приводит к развитию умеренной легочной гипертензии, когда среднее давление в легочной артерии не превышает 50-55 мм рт. ст., а ЛСС остается нормальным. Это так называемая гиперволемическая форма легочной гипертензии. В дальнейшем возникает спазм легочных сосудов, в связи с чем повышается ЛСС, что можно объяснить включением фактора эндотелиальной дисфункции с дисбалансом вазоактивных веществ и присоединением морфологических изменений легочных сосудов в виде пролиферации интимы, миэлоэластофиброза и т. д. В их развитии, возможно, имеют значение частые воспалительные процессы в бронхолегочной системе в детском возрасте из-за гиперволемии малого круга. Таким образом, в сложном патогенезе легочной гипертензии при ВПС важную роль играют факторы, которые приводят к ЛГ, ремоделированию сосудов легких и тромбообразованию:
- перегрузка левого предсердия;
- переполнение венозного русла легких;
- воспалительные процессы в легких;
- рефлекторный спазм артериол;
- эндотелиальная дисфункция.
Пусковые факторы в патогенезе идеопатической легочной гипертензии до конца не изучены. В настоящее время одной из известных причин является мутация гена BMPR2, которая обычно наследуется по аутосомно-доминантному типу. Эта форма называется семейной легочной артериальной гипертензией, частота ее выявления составляет менее 10% всех случаев легочной гипертензии. Обнаружен целый ряд возможных факторов риска развития спорадической формы ИЛГ: воздействие лекарственных препаратов и химических веществ, ВИЧ-инфекция, портальная гипертензия и др., которые обусловливают ее возникновение при наличии генетической предрасположенности. В настоящее время не вызывает сомнения тот факт, что идеопатическая легочная гипертензия — это группа клинических синдромов с разной этиологией. Считается, что легочная вазоконстрикция — ее ранний патогенетический механизм, в основе которого лежат нарушение функции калиевых каналов в гладкомышечных клетках и ЭД.
Довольно часто на амбулаторном приеме к семейному врачу или врачу-терапевту обращаются...
При легочной гипертензии, в первую очередь, нужно выполнять ряд общих рекомендаций: пациентам...
Тщательно собранный анамнез с учетом факторов окружающей среды, семейного анамнеза, вредных...
Причинами возникновения артериальной гипертензии могут быть заболевания аорты, такие как...
Наиболее распространенной причиной изолированной систолической артериальной гипертензии...
анализы, БАД, биологическая медицина, витамины, гастроэнтерология, гигиена, гинекология, гомеопатия, дерматология, диагностика, диетология, заболевания, иммунология, инфекционные заболевания, инфекция, исследования, кардиология, кожа, косметика, красота, лекарственные растения, лечение, лицо, неврология, обследование, оздоровление, онкология, ортопедия, педиатрия, питание, пищеварительная система, поведение, похудение, препараты, продукты, профилактика, процедура, психология, пульмонология, рак, реабилитация, сердечно-сосудистая система, ССС, тело, терапия, травматология, уход, фитотерапия, хирургия, эндокринология
Показать все теги

Комменатрии к новости