Ведение пациента с хроническим гепатитом B. Часть 4
До появления терапии нуклеотидными аналогами, рецидивирующая HBV-инфекция при трансплантации...
Специалистам / Практика / Практика (статья)
 ГепатитПРОДОЛЖЕНИЕ. НАЧАЛО ЗДЕСЬ: «Ведение пациента с хроническим гепатитом B. Часть 1»
ГепатитПРОДОЛЖЕНИЕ. НАЧАЛО ЗДЕСЬ: «Ведение пациента с хроническим гепатитом B. Часть 1»
Длительная монотерапия Энтекавиром и Тенофовиром ингибирует прогрессирование заболевания, оптимизирует гистологическую картину, снижает воспалительно-некротический компонент и проявление фиброза печени, часто способствует регрессии цирроза печени. Кроме этого, осложнения ранее существовавшего декомпенсированного цирроза, особенно на ранней стадии декомпенсации, уменьшались или даже исчезали, следовательно, исчезала потребность в трансплантации печени.
Тем не менее, развитие рака печени остается главной проблемой у пациентов с хронической HBV-инфекцией, которые принимают нуклеотидные аналоги. Как показывают проведенные рандомизированные и контролированные исследования, лечение с помощью нуклеотидных аналогов положительно влияет на частоту возникновения гепатоцеллюлярной карциномы. Полученные данные свидетельствуют о том, что после первых 5-ти лет терапии Энтекавиром или Тенофовиром у пациентов с хроническим гепатитом B показатель развития рака печени продолжает снижаться, причем снижение более очевидно у пациентов в начальной стадии цирроза печени. Кроме этого, рак печени с или без компенсированного циррозом, по-видимому, является единственным фактором, влияющим на долговременную выживаемость пациентов с хроническим гепатитом B, получавших Энтекавир или Тенофовир. Так как нуклеотидные аналоги используются при лечении большинства пациентов с хроническим гепатитом B, из-за их благоприятного воздействия на прогрессирование патологии, основной клинической проблемой является определение пациентов с риском развития рака печени, которые требуют тщательного наблюдения. Способность шкал оценки риска развития гепатоцеллюлярной карциномы у азиатских пациентов с хроническим гепатитом B (HCC, GAG-HCC, CU-HCC и REACH-B) оказалась ниже, чем при использовании шкалы PAGE-В, которая обеспечивает хорошую предсказуемость развития рака печени у кавказских пациентов с хроническим гепатитом В.
Основываясь на этих шкалах, пациентов можно классифицировать на низкий, средний и высокий риск развития рака печени. Пациенты с низкой вероятностью развития гепатоцеллюлярной карциномы не нуждаются в наблюдении.
Несмотря на постоянный риск развития рака печени, общие статистические данные улучшаются за счет пациентов, которые получают длительную эффективную терапию нуклеотидными аналогами. Снижение показателя HBsAg при длительной терапии нуклеотидными аналогами может произойти у немногих пациентов с хроническим гепатитом В, которые изначально были HBeAg-положительные (приблизительно 10-12% после 5-8 лет терапии), в то время как у пациентов с HBeAg-отрицательным хроническим гепатитом B – 1-2% после 5-8 лет терапии.
Показания преимущественного выбора Энтекавира или Тенофовир Алафенамид по сравнению с Тенофовир Дизопроксил Фумаратом
Отметим, что следует отдавать предпочтение Тенофовир Алафенамиду над Энтекавиром у пациентов с предшествующим приемом нуклеотидных аналогов
Так как терапия нуклеотидными аналогами обычно не приводит к ликвидации вируса гепатита B и редко приводит даже к элиминации HBsAg, сегодня разработаны долгосрочное терапевтическое схемы для большинства пациентов, которые получают лечение при хроническом гепатите В. Пациенты с HBeAg-положительным хроническим гепатитом В, которые принимали 6 или предпочтительней 12 месяцев консолидационную терапию, могут прекратить прием нуклеотидных аналогов, если они у них отмечается сероконверсия HBeAg и не обнаруживается ДНК HBV.
Согласно имеющимся данным, через 3 года после прекращения приема нуклеотидных аналогов у большинства пациентов (примерно 90%) отмечается сероконверсия HBeAg и вирусологическая ремиссия определяемая как ДНК HBV < 2000-20 000 МЕ/мл у примерно 50%. Следовательно, клиницисты могут самостоятельно определять необходимость продолжения терапии нуклеотидными аналогами до момента исчезновения HBsAg в анализе крови, что представляет собой самый безопасный результат завершения лечения.
Длительная терапия нуклеотидными аналогами рекомендуется HBeAg-отрицательным пациентам, которые смогут безопасно прекратить прием препаратов этой группы после наступления элиминация HBsAg. Доказательства, собранные в азиатских странах, свидетельствуют, что HBeAg-отрицательные пациенты с хроническим гепатитом B, у которых трижды не определяется ДНК HBV на протяжении 6 месяцев, могут прекратить прием нуклеотидных аналогов. Важным фактором, влияющим на вероятность вирусологической ремиссии вне лечения нуклеотидными аналогами, по-видимому, является отсутствие HBV ДНК в сыворотке во время терапии. В соответствии с существующими данными, вирусологическая ремиссия, определяемая как ДНК HBV < 2000-20 000 МЕ/мл наблюдается примерно у 50% пациентов через 3 года после прекращения приема нуклеотидных аналогов, если во время терапии на протяжении более двух лет отмечалась вирусологическая ремиссия. Так как эти выводы основаны на исследованиях с продолжительностью вирусологической ремиссии во время терапии от 2 до 5 лет, остается не ясным, какая оптимальная продолжительность лечения и сроки прекращения приема нуклеотидных аналогов для обретения устойчивой ремиссии. В настоящее время прекращение лечения с помощью нуклеотидных аналогов не рекомендуется пациентам с циррозом печени, так как вспышки явного гепатита и опасные для жизни осложнения изредка возникали у больных с ранее существовавшим циррозом, которые прекращали прием нуклеотидных аналогов. Более того, прием нуклеотидных аналогов может быть прекращен только у пациентов, которые имеют возможность внимательно следить за уровнем активности АЛТ и контролировать уровень ДНК HBV как минимум в течение первого года после прекращения приема нуклеотидных аналогов. К сожалению, нет достоверного маркера, который мог бы предсказать, когда именно наступит ремиссия после назначения нуклеотидных аналогов. На данный момент, еще не определены точные критерии назначения повторного лечения. Опираясь на данные клинических заключений, показания к лечению для пациентов с хроническим гепатитом В такие же, как и у пациентов, которые прекратили прием нуклеотидных аналогов.
Профилактика развития резистентности основана на использовании в первую очередь нуклеотидных аналогов с высоким барьером резистентности и максимальной способностью подавления вируса. Следует избегать сочетания нуклеотидных аналогов с низким барьером к резистентности (Ламивудин или Телбивудин с Адефовиром), так как это может привести к неадекватному подавлению вируса и появлению полирезистентных штаммов. Также следует строго избегать последовательную монотерапию препаратами с низким барьером резистентности из-за высокого риска формирования полирезистентных штаммов.
Неудачная терапия нуклеотидными аналогами у пациентов с хроническим гепатитом B остается важнейшей проблемой в странах, где Энтекавир, Тенофовир и Тенофовир Алафенамид недоступны, в отличие от стран, где нуклеотидные аналоги с высоким барьером резистентности используются в течение многих лет и случаи неудачного лечения у пациентов минимизированы.
Неэффективное лечения может быть в трех вариантах:
|
Тип резистентности |
Стратегия лечения |
|
Резистентность к Ламивудину |
Переход на Тенофовир или Тенофовир Алафенамид |
|
Резистентность к Телбивудину |
Переход на Тенофовир или Тенофовир Алафенамид |
|
Резистентность к Энтекавиру |
Переход на Тенофовир или Тенофовир Алафенамид |
|
Резистентность к Адефовиру |
-Если до этого пациент не получал Ламивудин – переход на Энтекавир, на Тенофовир или Тенофовир Алафенамид -Если пациент резистентный к Ламивудину – переход на Тенофовир или Тенофовир Алафенамид -Если уровень ДНК HBV низкий – добавить Энтекавир (собенно у пациентов резистентным к Адефовиру с мутациями (rA181T / V и/или rN236T) и с высокой вирусной нагрузкой, ответ на Тенофовир или Тенофовир Алафенамид может быть затяжным) или переход на Энтекавир |
|
Резистентность к Тенофовиру и/или Тенофовир Алафенамиду (Клинически не наблюдалось; нужно сделать генотипирование и фенотипирование для определения профиля перекрестной резистентности) |
-Если пациент до этого не принимал Ламивудин – переход на Энтекавир -Если пациент резистентен к Ламивудину – добавить Энтекавир (Долгосрочная безопасность этих комбинаций неизвестна) |
|
Полирезистентность |
Переход на комбинацию Энтекавир + Тенофовир или Тенофовир Алафенамид |
В последнее время, противовирусная резистентность стала управляемой. Риск резистентности связан с высоким исходным уровнем ДНК HBV, медленным снижение ДНК HBV и предыдущим неудачным лечением нуклеотидными аналогами. Резистентность должна быть идентифицирована путем контроля уровня ДНК HBV, в идеале – обнаружение картины резистентной мутации, после чего рекомендуется менять стратегию лечения. При обнаружении резистентности адекватная заместительная терапия должна быть начата с наиболее эффективного противовирусного препарата, который не имеет перекрестной резистентности, чтобы минимизировать риск возникновения лекарственно-устойчивых штаммов. У пациентов с лекарственной мультирезистентностью, должен проводится тест определения генотипической резистентности. В таких случаях сочетание Тенофовира с Энтекавиром оценивается как лучший вариант терапии.
Лечение PegIFNα может рассматриваться только у пациентов с хроническим гепатитом В от легкой до средней степени тяжести и, возможно, некоторых пациентов с компенсированным циррозом печени, но без портальной гипертензии. У 20-30% HBeAg-положительных пациентов с хроническим гепатитом B ответ на лечение наступает через 6 и 12 месяцев терапии PegIFNα. Хотя большинство пациентов реагируют элиминацией HBeAg или сероконверсией в течение первых 6 месяцев терапии, курс лечения длится более 6 месяцев PegIFNα; более низкие дозы рекомендуются для проведения 12-месячного курса лечения. Комбинированный конечный результат элиминации HBeAg с HBV ДНК < 2000 МЕ/мл через 6 месяцев после лечения был достигнут в 23% при метаанализе трех крупных исследований. Среди пациентов, которые достигли потери HBeAg через 6 месяцев после лечения, отрицательность HBeAg сохранялась 3 года после лечения в 81% случаев. Скорость элиминации HBsAg после 12 месяцев лечения составляла 3-7%. Элиминация HBsAg увеличиваются после окончания терапии PegIFNα у первоначально HBeAg-положительных пациентов с хроническим гепатитом B с устойчивым вирусологическим ответом. В группе пациентов с начальной элиминацией HBeAg, 30% испытали абсолютную элиминацию HBsAg через 3 года во время наблюдения. Были описаны случаи устойчивой потери HBsAg и сероконверсии после лечения PegIFNα.
Исследования показали, что у HBeAg-отрицательных пациентов с хроническим гепатитом B 48-недельная терапия PegIFNα обеспечивала устойчивый биохимический и вирусологический ответ у 60% и 44% больных через 6 месяцев, и 31% и 28% через 3 года после окончания терапии. Использование PegIFNα было менее эффективным у HBeAg-отрицательных пациентов с генотипом D или E, которые обрели вирусологический ответ в 20%. Немного исследований было проведено для рассмотрения эффективности PegIFNα у HBeAg-отрицательных пациентов с хроническим гепатитом В с генотипом B или C. В ретроспективном корейском исследовании приблизительно 30% HBeAg-отрицательных пациентов с генотипом C достигли вирусологический ответ через 1 год после окончания терапии PegIFNα.
Во время регистрационного исследования, элиминация HBsAg редко возникала во время терапии PegIFNα у HBeAg-отрицательных пациентов с хроническим гепатитом B, но скорость прогрессирования элиминации HBsAg после отмены PegIFNα была следующей: с 3% на 6 месяце до 9% в год, с 3 до 12% на 5-й год 1. Аналогичные показатели были подтверждены исследованиями в реальной клинической практике. В целом, среди устойчивых пациентов примерно 30% обрели элиминацию HBsAg в отдаленном времени.
В двух исследованиях была проведена оценка безопасности и эффективности длительной терапии PegIFNα, сроком более 48 недель у HBeAg-отрицательных пациентов с хроническим гепатитом B. В европейском рандомизированном исследовании, в котором преобладали пациенты с генотипом D, 96-ти недельная терапия PegIFNα, по сравнению с 48-ми недельной, продемонстрировала более высокие показатели устойчивого вирусологического ответа (29% против 12%, p = 0,03) и элиминации HBsAg (6% против 0%). Аналогичным образом, китайское исследование, с HBeAg-отрицательными пациентами с генотипом B или C показали, что 72 недельное лечение PegIFNα, по сравнению с 48 недельным, привело к более высоким уровням устойчивого вирусологического ответа (50% против 16%, p = 0,001) и элиминация HBsAg (36% против 10%, p <0,05).
Пациенты, получавшие PegIFNα, должны регулярно сдавать общий анализ крови, проверять уровень активности АЛТ ежемесячно и определять уровень ТТГ каждые 3 месяца. Все пациенты должны быть под наблюдением на протяжении 12 месяцев после лечения. ДНК HBV сыворотки и уровень HBsAg у всех пациентов с хроническим гепатитом B, HBeAg и анти-HBe у HBeAg-положительных пациентов с с хроническим гепатитом B следует проверять на 3, 6 и 12 месяце лечения PegIFNα, а также через 6 и 12 месяцев после завершения лечения. Конечной и самой желаемой точкой лечения HBeAg-положительных пациентов с хроническим гепатитом В является устойчивый уровень ДНК HBV < 2000 МЕ/мл в сыворотке, или даже лучше элиминация HBsAg вместе с нормализацией АЛТ у всех пациентов с хроническим гепатитом В, а также сероконверсия HBeAg. Устойчивый вирусологический ответ после PegIFNα обычно ассоциируется с ремиссией заболевания печени, всем HBeAg-положительным пациентам требуется долгосрочное наблюдение из-за риска обострения заболевания с развитием HBeAg-отрицательного хронического гепатита В или даже серореверсии HBeAg. Вероятность реактивации HBV, по-видимому, уменьшается со временем. У пациентов с неопределяемой ДНК HBV (и отрицательной HBeAg), через 12 месяцев следует проверять уровень HBsAg, так как скорость потери HBsAg увеличивается с течением времени. Пациентов, которые становятся HBsAg-отрицательными, следует регулярно проводить анализ на анти-HBs.
Предварительное лечение. У HBeAg-положительных пациентов с хроническим гепатитом B в качестве маркеров необходимости проведения предварительной терапии являются следующие показатели: высокий уровень активности АЛТ в сыворотке (выше верхнего показателя нормы в 2-5 раз), генотип HBV и показатели высокой активности процесса при биопсии печени. Было показано, что генотипы HBV A и B связанны с более высокими показателями сероконверсии HBeAg и HBsAg чем генотипы C и D.
У HBeAg-отрицательных пациентов с хроническим гепатитом B, с высоким исходным уровнем АЛТ, с низким исходным уровнем ДНК HBV, более молодым возрастом, женским полом и генотипом HBV были некоторые предикторы ответа на терапию PegIFNα, но информативность их оказалась низкой. Пациенты с генотипами B или C имели больше шансов на ответ на терапию, чем пациенты с генотипом D. Использование обобщенных данных из нескольких исследований во время терапии PegIFNα у HBeAg-отрицательных пациентов с хроническим гепатитом B, по бальной системе (от 0 до 7), которая объединяла пять характертстик (генотип HBV, ДНК HBV, уровень АЛТ, уровень HBsAg и возраст), позволила определить пациентов с высокой и низкой вероятностью ответа на терапию, но этот метод оценки еще не достаточно проверен. В настоящее время не рекомендуется использование в клинической практике базового генетического теста для определения приоритетности пациентов с хроническим гепатитом В для терапии PegIFNα, поскольку обнадеживающие результаты не были подтверждены в последующих исследованиях.
Период во время лечения. Самый важный предиктор ответа на лечение PegIFNα является уровень HBsAg в сыворотке, хотя он находится под влиянием генотипа HBV. У HBeAg-положительных пациентов с хроническим гепатитом В, снижение уровня HBsAg ниже 1500 МЕ/мл через 12 недель является точным предиктором сероконверсии HBeAg (положительное прогностическое значение составляет 50%), в то время как уровень HBsAg > 20 000 МЕ/мл для HBV с генотипом B и C, или отсутствие снижения уровня HBsAg для генотипа HBV A и D указывают на очень низкую вероятность последующей сероконверсии HBeAg. Если на 24-й неделе уровень HBsAg > 20 000 МЕ/мл, это значит что ответа на терапию не будет, независимо от генотипа вируса. Значительное снижение уровня ДНК HBV через 12 недель лечения дает 50% вероятностью сероконверсии HBeAg. Также, о частой сероконверсии HBeAg свидетельствуют колебания уровня HBeAg и иммунологически индуцированные колебания уровня активности АЛТ, при снижении уровня ДНК HBV. Однако клинически значимые снижения уровня HBV ДНК и HBeAg для прогнозирования ответа на лечение не были сообщены, они основаны на подтвержденных исследованиях и результатах исследований.
У HBeAg-отрицательных пациентов с хроническим гепатитом B сочетание недостатка снижения уровня HBsAg и уровень HBV ДНК < 210 МЕ/мл на 12 неделе лечения PegIFNα предсказывает об отсутствии ответа в генотипе D (отрицательное прогностическое значение: 100%). Это правило отмены терапии позволило бы прекратить использование PegIFNα примерно у 20% пациентов. На данный момент не существует надежных критериев отмены лечения для HBeAg-отрицательных больных хроническим гепатитом В с генотипами B или C, и очень малое количество доступных данных описано относительно генотипа A и E. В некоторых исследованиях также рассматривались положительные предикторы продолжительного ответа на лечение. Для HBeAg-отрицательных пациентов с хроническим гепатитом В с любым генотипом, кроме D, снижение уровня сывороточного HBsAg ≥ 10% от исходного уровня до 12 недели лечения PegIFNα указывает на высокую вероятность достижения устойчивого ответа на лечение, чем у пациентов с 10%-ным снижением (47% против 16%, p < 0,01), но, в данном случае, положительное прогностическое значение оказалось низким (~50%).
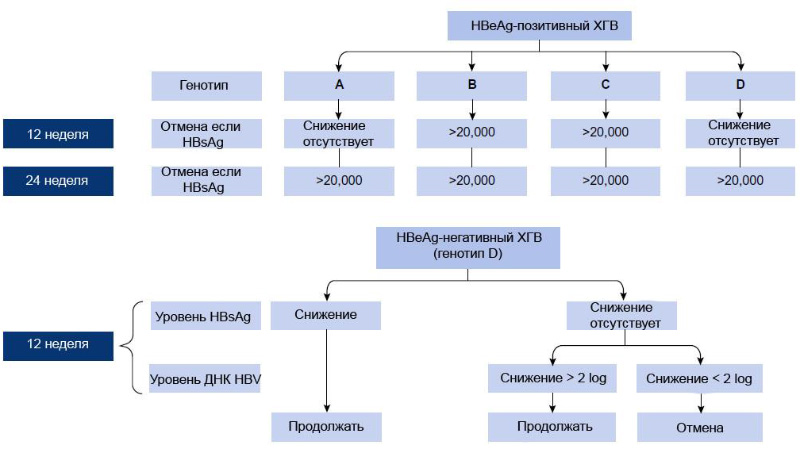
Рисунок 2. Правила отмены PegIFNα у HBeAg-положительных и отрицательных пациентов на 12 и 24 неделе терапии (правила основаны на показателе вирусного генотипа HBsAg и уровня HBV)
Лечение гепатита B PegIFNα имеет значительное количество побочных эффектов, хотя пациенты с HBV-инфекцией терпят это неудобство, так как большинство из них в молодом возрасте и имеют меньше сопутствующих патологий, чем пациенты с хроническим гепатитом B. Чаще всего возникают побочные эффекты характеризующиеся гриппоподобным синдромом, миалгией, головной болью, усталостью, потерей массы тела, депрессией, выпадением волос и местными реакциями в месте инъекции препарата. Могут возникнуть вспышки гепатита, которые приводят к декомпенсации болезни печени, поэтому PegIFNα противопоказан пациентам с декомпенсированным циррозом печени. Лечение PegIFNα также приводит к умеренной миелосупрессии, но нейтропения и тромбоцитопения обычно хорошо контролируется с помощью уменьшения дозы (иногда возникает клинически значимый инфекционный процесс или кровотечение). Комбинация PegIFNα с Телбивудином противопоказана из-за высокого риска развития нейропатии.
Большинство пациентов с устойчивым ответом на лечение IFNα или PegIFNα поддерживают этот ответ в течение длительного периода, продолжительностью не менее 5 лет. У пациентов с устойчивым ответом на лечение не отмечается прогрессирование патологии печени, а базовые гистологические показатели печени улучшаются. Тем не менее, остается риск развития гепатоцеллюлярной карциномы после терапии PegIFNα, даже у пациентов с устойчивой реакцией на лечение, особенно при наличии цирроза. Как оказалось, при лечении азиатских пациентов, терапия PegIFNα имеет преимущество над терапией нуклеотидными аналогами в отношении лечения гепатоцеллюлярной карциноме. Кроме этого, старые когортные исследования и систематические обзоры cо стандартным лечением INFα показывают, что риск развития рака печени снижается при лечении IFNα по сравнению с пациентами, которые не получили лечения хронического гепатита В (такой эффект более ясен у азиатских пациентов и у тех, кто продолжительно не принимал лечения, и/или у пациентов с компенсированным циррозом). Когортные исследования с HBeAg-положительными и с HBeAg-отрицательными пациентами с хроническим гепатитом B показали, что курсы стандартного лечение IFNα приводят к улучшению общих долгосрочных результатов, в том числе и выживаемости пациентов с длительным отсутствием лечения. Данные о выживаемости пациентов на фоне лечения PegIFNα, к сожалению, недоступны, но ожидаются благоприятные результаты, если достигается устойчивый ответ после завершения лечения. Скорости элиминации HBsAg у резистентных пациентов постепенно приближаются к 50% через 5 лет после окончания терапии.
Было проведено лишь несколько исследований, оценивающих роль комбинированной терапии с мощными нуклеотидными аналогами при лечении хронической HBV-инфекции. В большом перспективном многоцентровом исследовании, HBeAg-положительные и -отрицательные пациенты с хроническим гепатитом B были рандомизированы к лечению Энтекавиром или Энтекавиром + Тенофовиром. Первичная конечная точка (HBV ДНК < 50 МЕ/мл на 96 неделе) была достигнута у 76% и 83% пациентов, получавшие моно- или комбинированную терапию, соответственно (Р = 0,088). В подгруппе с HBeAg-положительными пациентами комбинация Энтекавира / Тенофовира достигла значительно высших показателей ДНК HBV > 50 МЕ/мл (80% по сравнению с 70%, p = 0,046), что было полностью обусловлено базовым уровнем ДНК HBV ≥ 108 МЕ/мл у HBeAg-положительной подгруппе пациентов (79% против 62%). Однако никакой разницы не было обнаружено в скорости сероконверсии HBeAg. Ни один из пациентов не обрел резистентности, тогда как нормализация АЛТ наблюдалась чаще в группе монотерапии энтекавиром (82% против 69%). Эта комбинация не обеспечила весомого значения в изменчивости уровня HBsAg.
Во втором двойном рандомизированном исследовании, лечение HBeAg-положительных пациентов с высоким показателем уровня ДНК HBV и нормальными уровнями АЛТ проводилось либо комбинацией с Тенофовиром + плацебо, либо комбинацией из Тенофовира + Эмтрицитабин в течение 192 недель. На 192 неделе у 55% и 76% пациентов с монотерапией Тенофовиром и у группы пациентов с комбинированной терапией соответственно было достигнуто: HBV ДНК < 69 МЕ/мл (р = 0,016). Те, кто не достиг таких данных, были низкие уровни продолжающейся репликации HBV с уровнем ДНК HBV в сыворотке < 500 МЕ/мл. Однако сероконверсия HBeAg наблюдалась только у 5% пациентов (все из группы монотерапии), в то время как ни один пациент не обрел устойчивости к вирусу гепатита В.
Хотя оба вышеуказанных исследования показали более высокий процент полного подавления ДНК HBV во время комбинации терапии нуклеотидными аналогами, у HBeAg-положительных пациентов с высокой исходной вирусной нагрузкой (ДНК HBV > 108 МЕ/мл) колебания уровня ДНК HBV во время лечения и клинические / серологические ответы наблюдаемые в обеих стратегиях, недостаточно сильны, чтобы рекомендовать этот метод лечения для таких пациентов.
Вопрос оптимального ведения пациентов с неполным подавлением репликации HBV при длительном применении (Энтекавира, Тенофовира или Тенофовир Алафенамид) все еще остается предметом дебатов. У большинства таких пациентов непрерывное снижение уровня ДНК HBV может наблюдаться при продолжении действия того же самого препарата. Крупные долгосрочные исследования доказали, что такой подход к лечению является безопасным, эффективным и не приводит к развитию резистентности к лекарственным средствам. До сих пор нет убедительных данных, которые бы демонстрировали, что наличие минимальной остаточной виремии с уровнем ДНК HBV < 69 МЕ/мл может иметь какой-либо неблагоприятный эффект в отношении прогрессирования заболевания на стадии лечения или риска развития рака печени у пациентов без цирроза. Поэтому не рекомендуется изменять принципам первоначальной стратегии лечения у пациентов с низким уровнем и/или с низким показателем уровня ДНК вируса гепатита В на фоне мощной монотерапии нуклеотидными аналогами.
Но было доказано, что у пациентов с декомпенсированным циррозом печени, достижение вирусологического ответа, определяемого как ДНК HBV < 20 МЕ/мл, является существенным фактором риска для развития рака печени (HR = 7,74, 95% 1,CL 1.34-44,78, р = 0,022), чем у больных с компенсированным циррозом (p = 0,749) .
Причиной долгосрочных колебаний уровня ДНК HBV во время лечения выше 69 МЕ/мл и ниже 2000 МЕ/мл, не известна. Поскольку вышеупомянутые исследования показали некоторые преимущества комбинации нуклеотидных аналогов в период подавления ДНК HBV, эту тактику лечения рекомендуется применять пациентам с установленным диагнозом цирроза печени. Ретроспективное исследование лечения Энтекавиром (суточная доза 0,5 мг) показало, что при добавлении Тенофовира к Энтекавиру или повышение дозы Энтекавира до 1,0 мг при лечении больных с неполным ответом ДНК HBV, происходит нормализация уровня АЛТ, по сравнению с монотерапией Энтекавиром в дозе 0,5. Замена препарата на более мощный нуклеотидный аналог (т.е. смена Энтекавира на Тенофовир / Тенофовир Алафенамид или наоборот) также может привести к улучшенному ответу на лечение.
Комбинация нуклеотидных аналогов и PegIFNα была использована в лечении подавленных к нуклеотидным аналогам пациентов с хроническим гепатитом B. Нет убедительных доказательств того, что для лечения пациентов комбинация PegIFNα и нуклеотидных аналогов чем-то превосходит использование PegIFNα или нуклеотидных аналогов как монотерапию. Предыдущие исследования комбинации PegIFNα с Ламивудином и/или Адефовиром не смогли показать преимущества комбинированной терапии. Рандомизированное контролируемое исследование показало, что у пациентов, которые принимали PegIFNα и Тенофовир Дизопроксил Фумарат, 72-недельная элиминация HBsAg показало личшие результаты по сравнению с пациентами, получавшими PegIFNα или Тенофовир (9%, 3% и 0% соответственно), но общие показатели были низкими, главным образом у пациентов с генотипом А. Для ведения пациентов, не получавших раньше никакого лечения, нет убедительных доказательств того, что кратковременная предварительная терапия нуклеотидными аналогами улучшит темпы устойчивого реагирования на PegIFNα. Многоцентровое исследование ARES продемонстрировало, что 24-недельный курс PegIFNα, предоставленный небольшой группе HBeAg-положительных пациентов, которые принимали только терапию Энтекавиром на протяжении 24 недель, может улучшить падение уровня HBeAg, ДНК HBV и HBsAg, по сравнению с монотерапией Этеновиром, но монотерапевтический эффект PegIFNα отсутствует.
У пациентов с хроническим гепатитом B при длительной эффективной вирусологической ремиссии во время терапии нуклеотидными аналогами, PegINFα может использоваться как дополнение к основной терапии, или можно перейти с нуклеотидных аналогов на PegINFα. Два китайских исследования оценивали эффективность и безопасность перехода пациентов на терапию на PegIFNα после длительной и эффективной терапии нуклеотидными аналогами. После 48-недельного курса РegIFNα у 6-20% пациентов отмечалось снижение уровня HBsAg. При проведении серологических реакций базовый уровень HBsAg < 1,500 МЕ/мл. Два азиатских исследования оценили 48-недельный курс терапии PegIFNα и длительной терапии нуклеотидными аналогами у HBeAg-положительных пациентов. Уровень элиминации HBsAg существенно не увеличивался, в то время как снижение уровня HBsAg было больше в группе, где проводили комбинированную терапию.
Два Многоцентровых европейских исследования оценили безопасность и эффективности 48-недельного дополнительного курса PegIFNα у HBeAg-отрицательных пациентов с хроническим гепатитом В при лечении нуклеотидными аналогами показали, что снижение HBsAg усиливалось при добавление PegIFNα, но только несколько пациентов обрели элиминацию HBsAg. Уровень HBsAg перед началом исследования и на 12 неделе свидетельствует о снижение HBsAg и/или полной элиминации HBsAg. Нет исследований, посвященных оценке безопасности и эффективности перехода на монотерапию PegIFNα для HBeAg-отрицательных пациентов с хроническим гепатитом B при длительной терапии нуклеотидными аналогами.
По завершению PegIFNα-терапии, пациенты нуждались в длительной терапии нуклеотидными аналогами; этот факт увеличивает стоимость терапии PegIFNα, также не стоит забывать о побочных эффектах лечения с помощью PegIFNα. Именно поэтому следует тщательно оценивать все возможные преимущества и недостатки этой стратегии терапии.
Пациентов с декомпенсированным циррозом следует направлять на трансплантацию печени и лечить с помощью нуклеотидных аналогов как можно раньше, с целью достижения полного подавления вируса в кратчайшие сроки. Энтекавир или Тенофовир являются предпочтительными препаратами лечения – оба препарата эффективны и, как правило, безопасны для пациентов с декомпенсированной патологией. Рекомендуемая доза Энтекавира для пациентов с HBV и декомпенсированым циррозом – 1 мг (вместо 0,5 мг для пациентов с компенсированным циррозом) 1 раз в день. При этом не рекомендуется использовать менее мощные нуклеотидные аналоги, так как они не продемонстрировали желательного эффекта по сравнению с более мощными препаратами. Несмотря на общую безопасность применения нуклеотидных аналогов, есть опасения, что развитие молочного ацидоза у пациентов с декомпенсированным циррозом развивается именно на почве лечения нуклеотидными аналогами, поэтому пациентам с баллом MELD < 22 рекомендуется тщательное наблюдение для профилактики повреждения функции почек. Все дозы нуклеотидных аналогов должны быть скорректированы в соответствии с функцией почек. Благодаря благоприятному профилю безопасности, Тенофовир может использоваться как вариант лечения пациентов с декомпенсированной патологией печени, особенно у лиц с дисфункцией почек. Однако, исследования, подтверждающие безопасность и эффективность Тенофовира для таких пациентов, не проводились. PegIFNα противопоказан пациентам с декомпенсированной патологией печени.
Основная цель лечения нуклеотидными аналогами у пациентов с декомпенсированным циррозом печени – достижение клинической компенсации с последующей трансплантацией печени. Есть убедительные доказательства того, что противовирусная терапия значительно изменяет естественное течение декомпенсированного цирроза печени, улучшает функцию печени и увеличивает выживаемость. Собраны данные общей выживаемости пациентов на фоне лечения нуклеотидными аналогами без трансплантации печени (количество таких пациентов составляет 80%). Примерно 35% пациентов, которые принимали нуклеотидные аналоги, были вычеркнуты со списка ожидания на трансплантацию печени (отмечалось улучшение по классификации Чайлда-Пью [Child-Pugh] ≥ 2 наблюдается по меньшей у 40-50% больных). Пациенты с ранним лечением имеют лучшие клинические результаты, чем пациенты с отсроченным лечением. Высокий балл по шкале Child-Pugh или MELD является предиктором плохой выживаемости. Улучшение показателей MELD или Child-Pugh на раннем этапе лечения прогнозирует высокую выживаемость без проведения трансплантации печени. Неопределяемый уровень ДНК HBV может быть достигнут у > 80% больных после 1 года лечения, и уменьшает риск развития рака печени. Всем пациентам с декомпенсированным циррозом рекомендуется пожизненное лечение. Даже при эффективной терапии нуклеотидными аналогами, риск развития гепатоцеллюлярной карциномы у этих пациентов достаточно высокий. Долгосрочное наблюдение пациентов с раком печени является обязательным.
ПРОДОЛЖЕНИЕ ЗДЕСЬ: «Ведение пациента с хроническим гепатитом B. Часть 4»
До появления терапии нуклеотидными аналогами, рецидивирующая HBV-инфекция при трансплантации...
Анализы на определение уровня тиреоидных и тиреотропного гормонов в крови назначают не...
Согласно данным всеукраинских общественных организаций, в Украине насчитывается примерно 5...
Вирусный гепатит С (ВГС) — одна из актуальных проблем современного здравоохранения. Это...
Хронический гепатит — это хронический воспалительный процесс в печени, который длится на...
анализы, БАД, биологическая медицина, витамины, гастроэнтерология, гигиена, гинекология, гомеопатия, дерматология, диагностика, диетология, заболевания, иммунология, инфекционные заболевания, инфекция, исследования, кардиология, кожа, косметика, красота, лекарственные растения, лечение, лицо, неврология, обследование, оздоровление, онкология, ортопедия, педиатрия, питание, пищеварительная система, поведение, похудение, препараты, продукты, профилактика, процедура, психология, пульмонология, рак, реабилитация, сердечно-сосудистая система, ССС, тело, терапия, травматология, уход, фитотерапия, хирургия, эндокринология
Показать все теги

Комменатрии к новости