Коморбидные состояния в перименопаузальный период
Перименопауза, или предклимактерический период, - это период репродуктивной жизни женщины,...
Специалистам / Практика / Практика (статья)
 ЭпилепсияДля клиницистов, проводящих лечение пациентов с эпилепсией, проблемой могут быть сложные, разнонаправленные взаимодействия между гормонами, эпилептическими приступами и лекарственными средствами, принимаемыми для контроля над ними. Многие гормоны действуют как нейростероиды, изменяя возбудимость головного мозга посредством прямого воздействия на сайты связывания. Следовательно, изменения уровня эндогенных или экзогенных гормонов могут воздействовать на развитие эпилептических приступов напрямую, а также опосредованно — путем фармакокинетического влияния, которое изменяет концентрацию антиэпилептических препаратов (АЭП). Лежащие в основе развития эпилепсии структурные и патофизиологические изменения головного мозга, а также метаболическая активность АЭП могут неблагоприятно влиять на функционирование гипоталамуса и гонад. Количество информации об этих сложных взаимодействиях возросло и в настоящее время эти знания могут быть включены в разработку эффективных подходов к лечению эпилепсии у мужчин и женщин.
ЭпилепсияДля клиницистов, проводящих лечение пациентов с эпилепсией, проблемой могут быть сложные, разнонаправленные взаимодействия между гормонами, эпилептическими приступами и лекарственными средствами, принимаемыми для контроля над ними. Многие гормоны действуют как нейростероиды, изменяя возбудимость головного мозга посредством прямого воздействия на сайты связывания. Следовательно, изменения уровня эндогенных или экзогенных гормонов могут воздействовать на развитие эпилептических приступов напрямую, а также опосредованно — путем фармакокинетического влияния, которое изменяет концентрацию антиэпилептических препаратов (АЭП). Лежащие в основе развития эпилепсии структурные и патофизиологические изменения головного мозга, а также метаболическая активность АЭП могут неблагоприятно влиять на функционирование гипоталамуса и гонад. Количество информации об этих сложных взаимодействиях возросло и в настоящее время эти знания могут быть включены в разработку эффективных подходов к лечению эпилепсии у мужчин и женщин.
Неврологами давно принято, что гормоны различными путями участвуют в проявлениях эпилепсии и в ее лечении АЭП. Например, определение повышенной концентрации пролактина в сыворотке крови после события, напоминающего эпилептический приступ, используется при проведении дифференциальной диагностики эпилептического приступа и неэпилептического события. Кроме того, лечение инфантильных спазмов при помощи адренокортикотропного гормона является стандартным подходом. Эти относительно распространенные варианты обычно не воспринимаются как часть нейроэндокринологии, но они ясно подтверждают наличие связи между нейростероидными гормонами и эпилепсией.
Динамическая роль гормонов при эпилепсии разноплановая, с вовлечением множества факторов. В этой статье описаны результаты основных исследований по изучению нейростероидов в контексте эпилепсии, нарушению гипоталамической гормональной регуляции при эпилепсии, а также влиянию АЭП на гормоны репродуктивной системы. На рис. 1 представлены гипоталамо-гипофизарная ось у женщин и мужчин, в том числе гормоны, имеющие отношение к тематике этой статьи. Обсуждены относящиеся к вопросу клинические варианты, в том числе катамениальная эпилепсия (приступы, связанные с менструальным циклом), синдром поликистозных яичников (СПКЯ), проблемы фертильности, перименопаузального и менопаузального периодов. Варианты тактики ведения пациентов предложены с учетом результатов, представленных в следующих разделах.
 Гипоталамо-гипофизарная ось у женщин и мужчин
Гипоталамо-гипофизарная ось у женщин и мужчин
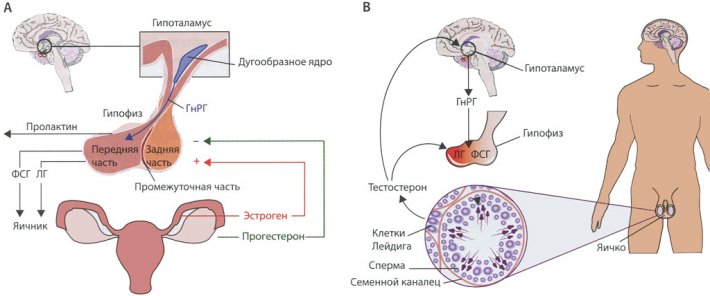
Рисунок 1. Гипоталамо-гипофизарная ось у женщин и мужчин.
Гормоны, имеющие отношение к тематике данной статьи, показаны у женщин (А) и мужчин (В).
ФСГ – фолликулостимулирующий гормон.
ЛГ – лютеинизирующий гормон.
ГнРГ – гонадотропин-рилизинг гормон.
Нейростероиды представляют собой молекулы стероидов, которые оказывают модулирующее воздействие на возбудимость головного мозга и, следовательно, могут влиять на развитие приступов. Эстроген и прогестерон, основные половые гормоны женщин, влияют на нейрональную возбудимость. Сложное воздействие эстрогена на нервную возбудимость осуществляется посредством двух механизмов. К первому относят негеномное воздействие с коротким латентным периодом, которое предположительно опосредуется через мембрану нейронов. Например, после воздействия 17β-эстрадиола на клетку гиппокампа при помощи метода локальной фиксации потенциала в конфигурации «whole cell» (Метод локальной фиксации потенциала (patch-clamp technique) – электрофизиологический метод локальной фиксации потенциала, используемый для изучения клеток, клеточных мембран, ионных каналов и, иногда, изолированных органелл; существуют различные модификации и конфигурации метода. Если по условиям эксперимента необходимо менять состав внеклеточной среды, используют конфигурацию «whole cell» («целая клетка»). В этом случае пипетку не отводят от клетки, а подают в нее отрицательное давление и таким образом разрушают изолированный фрагмент мембраны, при этом сохраняются клеточные структуры и регуляторные механизмы.) было выявлено усиление каинат-индуцированных токов. Такое воздействие имеет быстрое начало, является обратимым и дозозависимым, что соответствует мембранному эффекту. Ко второму, более тщательно изученному механизму, относят геномное воздействие с длительным (часы и дни) латентным периодом. Как и другие стероидные гормоны, эстроген пассивно проникает в клетку, где связывается с рецептором эстрогена и активирует его; рецептор представляет собой димерный ядерный белок, который связан с ДНК и контролирует генную экспрессию. После связывания эстрогена с рецептором этот комплекс образует фактор транскрипции, который связывается с гормон-чувствительными элементами генов и модифицирует клеточные ответные реакции. Примером этого воздействия служит эстрадиол-индуцированное повышение плотности сайтов связывания агонистов на NMDA-рецепторном комплексе (N-methyl-D-aspartate — N-метил-D-аспартат) в клетках гиппокампа, которое может быть зарегистрировано спустя 2 дня после начала лечения эстрадиолом. Давно было высказано предположение, что эстроген обладает проконвульсивными свойствами, но это влияние может быть более сложным, зависит от дозы, пути и кратности введения (однократного или длительного), природного гормонального фона и вида эстрогена. В целом в пределах физиологических концентраций эстроген, по-видимому, не является сильным проконвульсантом. Женщины с эпилепсией, однако, могут быть чувствительны к нейрофизиологическому проконвульсивному эффекту этого гормона в период стремительного эстрогенового пика, связанного с овуляцией.
При этом прогестерон, очевидно, способствует торможению нервной системы, в основном за счет воздействия его редуцированного метаболита аллопрегнанолона, который выступает положительным аллостерическим модулятором проводимости через ГАМК-ергические каналы. При исследовании на экспериментальных моделях установлено, что циклическое повышение и снижение концентрации прогестерона и аллопрегнанолона предсказуемо изменяло предрасположенность к развитию приступов, хотя неизвестно, объясняется ли полностью обострение катамениальных приступов этим циклическим гормональным влиянием.
Воздействие аллопрегнанолона на проводимость ГАМК-ергических каналов подчинено механизму обратной связи в пределах ГАМКА-рецептора. Компоненты субъединицы ГАМКA-рецептора подвергаются компенсаторным перестройкам в ответ на изменения эндогенных нейростероидов и при применении медикаментозных средств, оказывающих модулирующее влияние на ГАМКА-рецепторы, например, бензодиазепинов. Длительное воздействие аллопрегналона на крыс провоцирует усиление экспрессии α4-субъединицы ГАМКА-рецептора в гиппокампе, что приводит к снижению чувствительности ГАМКА- рецепторов к бензодиазепинам.
Другой основной половой гормон — тестостерон — также является нейростероидом. Тестостерон имеет два основных класса биологически активных метаболитов, оказывающих противоположное действие на нервную возбудимость: эстрогены, которые образуются под воздействием ароматазы, фермента системы цитохрома Р450, и 5α-редуцированные андрогены. Ароматаза и 5α-редуктаза экспрессируются в нескольких системах органов, в том числе и в головном мозге. 5α-Редуцированные андрогены оказывают преимущественно антиконвульсантный эффект, частично из-за их способности выступать в качестве субстратов для биосинтеза 5α-андростан- Зα-диола (5α-androstane-3α-diol — 3α-DIOL). Эта молекула структурно сходна с аллопрегнанолоном, образуется через сходный метаболический путь при помощи редукции и модулирует активность ГАМКА- рецептора таким же способом. Зα-DIOL синтезируется на периферии — в предстательной железе, печени и коже, а также глиальными клетками de novo в головном мозге. Установлено, что Зα-DIOL действует в зависимости от дозы как антиконвульсант при приступах у мышей, вызванных введением антагонистов ГАМКА-рецепторов — пентилентетразола, пикротоксина и сложного эфира (3-карболина. При изучении пентилентетразоловой модели приступов метаболит Зα-DIOL продемонстрировал мощный антиконвульсантный эффект. Потенциальная значимость Зα-DIOL для осуществления антиконвульсантного действия циркулирующих андрогенов была обнаружена на мышах с нокаутом гена 5α-редуктазы, у которых тестостерон не оказывал защитного влияния против приступов. Два других метаболита эндогенного тестостерона — андростерон и этиохоланолон, которые содержатся в довольно высоких концентрациях у мужчин, также обладают антиконвульсантными нейростеройдными свойствами. Оба метаболита продемонстрировали защитное действие против приступов у взрослых мышей мужского пола разной выраженности и в разных моделях, в том числе при воздействии 6 Гц электрической стимуляции, введении пентилентетразола, пилокарпина, 4-аминопиридина, по данным теста максимального электрошока, а также результатов исследования препаратов среза гиппокампа.
У женщин с эпилепсией отмечаются повышенные показатели развития СПКЯ и бесплодия, снижение либидо, а также раннее наступление менопаузы. Эпилепсия сама по себе действует как дезинтегратор работы эндокринной системы и приводит к развитию гипоталамической дисфункции, что в свою очередь, как правило, оказывает противоположное влияние на концентрацию андрогенов у мужчин и женщин — то есть у мужчин активность андрогенов снижается, а у женщин — повышается. Влияние эпилепсии на центральную репродуктивную деятельность сочетается с метаболическими нарушениями, вызванными воздействием АЭП на те половые гормоны, которые имеются и у мужчин и у женщин.
Области лимбической коры, в частности миндалевидное тело, имеют обширные реципрокные связи с гипоталамусом и могут оказывать модулирующее влияние на гипоталамо-гипофизарно-гонадную ось (рис. 1). У женщин и мужчин с эпилепсией наблюдается нарушение высвобождения гормонов гипофиза. Нарушение высвобождения фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ) развивается вслед за дисфункцией клеток гипоталамуса, продуцирующих гонадотропин-рилизинг гормон (ГнРГ). ГнРГ, вырабатываемый небольшим количеством клеток, расположенных преимущественно в преоптической области гипоталамуса, контролирует активность гонад посредством секреции пульсирующего типа и стимуляции высвобождения гормонов гипофиза.
Популяция ГнРГ-продуцирующих клеток уязвима к повреждению во время приступов. У крыс женского пола с приступами, индуцированными введением каиновой кислоты в миндалевидное тело, была отмечена ипсилатеральная потеря ГнРГ-окрашенных волокон в гипоталамусе. Латерализация височной эпилепсии, по-видимому, связана с определенными типами дисфункции половой системы. В ходе обследования 30 женщин со сложными парциальными приступами, у которых эпилептиформные разряды регистрировались в височных долях унилатерально, и были доказательства эндокринных нарушений репродуктивной системы, левосторонние разряды сочетались с СПКЯ, а правосторонние — с гипогонадотропным гипогонадизмом. Согласно определению последнее представляет собой эндокринопатию репродуктивной системы центрального (гипоталамического или гипофизарного) происхождения.
Как правило, АЭП, которые индуцируют печеночные ферменты метаболизма, известны как фермент-индуцирующие АЭП, и оказывают непосредственное влияние на изменение уровня половых гормонов (рамка 1). Они также индуцируют выработку глобулина, связывающего половые гормоны (ГСПГ), которые снижают концентрацию биологически активных (свободных) половых гормонов в сыворотке крови. Сообщалось о существенном повышении уровня ГСПГ у мужчин с фокальной эпилепсией, получавших карбамазепин и фенитоин, по сравнению с получавшими ламотриджин и здоровыми лицами группы контроля. Снижение уровня свободного тестостерона было отмечено у мужчин, принимающих карбамазепин, фенитоин, окскарбазепин и вальпроаты, и у лиц с парциальной эпилепсией, которым не проводили лечение.
|
Антиэпилептические препараты, которые снижают концентрацию стероидных половых гормонов: - Фенобарбитал Антиэпилептические препараты, которые незначительно снижают концентрацию стероидных половых гормонов: - Этосуксимид |
Прием вальпроатов обычно связан с повышением концентрации тестостерона. Сообщалось, что эти препараты индуцируют синтез андрогенов в яичниках. Предложено несколько механизмов ингибирования, вносящих свой вклад в такое действие, и они могут иметь значение как для мужчин, так и для женщин: прямое ингибирование изоферментов 2С9 и 2С19 цитохрома Р450, которые метаболизируют образование андростендиона из тестостерона; ингибирование ароматазы, которая превращает тестостерон в эстрадиол; и ингибирование эпоксидгидролазы, которая также может выступать как фермент, опосредующий превращение тестостерона в эстроген, как было показано при культивации зернистых клетках яичника человека. У женщин такая ингибиторная активность вальпроатов оказывает отчетливо неблагоприятное влияние на репродуктивную систему. В норме зернистые клетки секретируют тестостерон и окружают фолликул яичника, когда он созревает для овуляции. Эти клетки продуцируют постепенно возрастающее количество эстрогена путем ферментативного превращения его из тестостерона до достижения пика концентрации эстрогена, связанного с овуляцией. Фолликул сам по себе является объектом для стимуляции ФСГ, который обеспечивает развитие фолликула. Ферментативное ингибирование нормальной продукции гормонов яичником приводит к формированию незрелого, неовулирующего фолликула, который секретирует тестостерон. Этот механизм может объяснить, как вальпроаты приводят к развитию состояния гиперандрогении, а также отсутствию овуляции и формированию кист яичников. Воздействие вальпроатов при их пероральном введении крысам мужского и женского пола приводило к изменению морфологии гонад: у крыс женского пола формировались кисты яичников, а у мужского — возникала атрофия яичек. У животных обоего пола прием вальпроатов был связан со снижением концентрации эстрогена, неизменным уровнем тестостерона, а также повышенным уровнем ФСГ и ЛГ в сыворотке крови. Центральное и периферическое ингибирование ароматазы может объяснить такое влияние.
Lofgren et а1. сообщили о снижении концентрации общего тестостерона и индекса свободных андрогенов (100хконцентрация тестостерона/концентрация ГСПГ) у женщин с эпилепсией, которые принимали карбамазепин или окскарбазепин. Однако АЭП, которые не являются индукторами метаболических ферментов печени, оказывают незначительное влияние на андрогены. Lossius et а1. пришли к выводу, что влияние фермент-индуцирующих АЭП является обратимым: после отмены карбамазепина концентрация общего тестостерона и индекс свободных андрогенов статистически значимо повысились и у мужчин, и у женщин. Кроме того, после прекращения приема карбамазепина уровни 17β-эстрадиола и прогестерона статистически значимо повысились у мужчин, но не у женщин.
Прием леветирацетама, который связывается с рецептором SV2А, представленном в головном мозге, в тканях гонад и эндокринной системы, был связан с повышением уровня общего тестостерона у мужчин при оценке спустя 1 мес после начала лечения.
Концентрации ЛГ и ФСГ не изменялись, что указывает на прямое воздействие на гонады. По результатам поперечного исследования с участием мужчин и женщин с эпилепсией не было выявлено различий в уровнях гормонов репродуктивной системы между группами, принимающими карбамазепин, ламотриджин и леветирацетам. Однако у принимающих карбамазепин были ниже индекс свободных андрогенов и уровень дегидроэпиандростерон-сульфата, а также повышен уровень глобулина, связывающего стероидные гормоны, ФСГ и ЛГ, по сравнению с показателями у принимавших другие лекарственные средства. Тем не менее результаты этих двух исследований не столь противоречивы, как представляется: в более раннем исследовании оценивали изменения с течением времени после начала лечения леветирацетамом, а в проведенном позднее концентрацию определяли у каждого пациента только один раз.
Кластеры приступов, коррелирующие с началом менструации, определяются как катамениальные; этот термин произошел от греческого слова katamenios, что означает ежемесячный. Сэр Charles Locock в 1857 г. впервые описал приступы, связанные с менструальным циклом. Есть сведения об обострении приступов в менструальный период в связи с колебаниями концентрации эндогенных гормонов приблизительно у 70% женщин с эпилепсией, но может быть затруднительно установить связь между менструацией и приступами, поскольку приступы носят кластерный характер у многих пациентов, как у мужчин, так и у женщин, без ассоциации с менструальным циклом.
В среднем менструальный цикл составляет 28 дней (варьирует от 24 до 35 дней), при этом первый его день соответствует первому дню менструации, а овуляция приходится на 14-й день. В менструальном цикле выделяют две фазы: фолликулярную (1—14-й день) и лютеиновую (15-28-й). В фолликулярную фазу фолликулы в яичнике растут, и доминантный фолликул с наибольшим количеством фолликулярных рецепторов становится овуляторным фолликулом, содержащим ооцит. На 14-й день ооцит высвобождается (овуляция) и недоминантные фолликулы подвергаются обратному развитию. В лютеиновую фазу доминантный фолликул формирует желтое тело, продуцирующее прогестерон. На рис. 2 показаны колебания эстрадиола и прогестерона в период нормального менструального цикла, а также при ановуляторном менструальном цикле с нарушением лютеиновой фазы. Представлены колебания уровня гормонов, имеющие наибольшее значение для обострения катамениальных приступов: начало быстрого нарастания концентрации эстрогена на 13-й день, которое инициирует овуляцию, и быстрое снижение концентрации прогестерона, а затем и эстрогена к 26-28-му дню, как раз перед началом менструального кровотечения.
 Паттерны катамениальной эпилепсии
Паттерны катамениальной эпилепсии
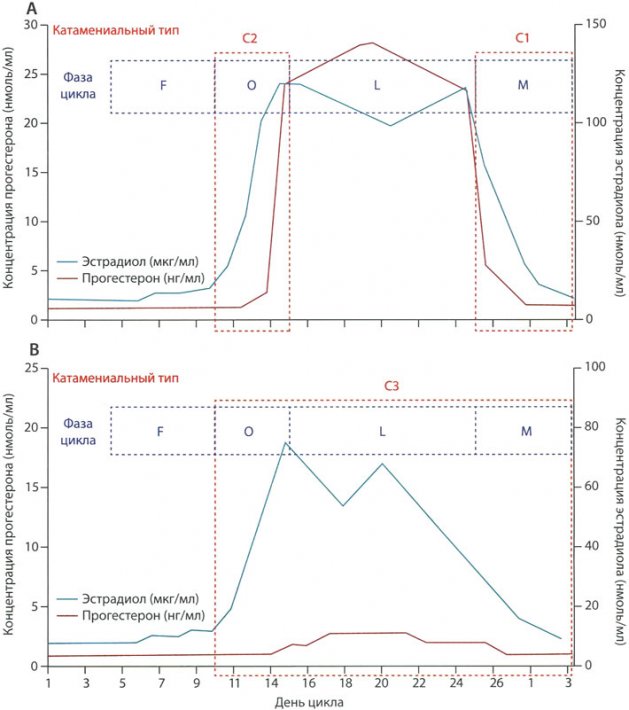
Рисунок 2. Паттерны катамениальной эпилепсии
(А) Нормальный цикл. Паттерны С1 и С2 связаны с обострением приступов во второй половине цикла (14-28-й день) после нормальной овуляции.
(В) Цикл с нарушением лютеиновой фазы. Паттерн С3 связан с обострением в период недостаточности лютеиновой фазы, при этом за первый день принят первый день менструального цикла, а овуляция приходится на 14-й день.
С (catamenial seizure pattern) – паттерн катамениального приступа.
F (follicular phase) – фолликулярная фаза.
О (periovulatory) – периовуляторный период.
L (luteal phase) – лютеиновая фаза.
М (perimenstrual) – перименструальный период.
Нарушение регуляции секреции ФСГ приводит к недостаточному развитию фолликула и, следовательно, к плохому функционированию желтого тела, что является нарушением, известным как недостаточность лютеиновой фазы, и связано с отсутствием овуляции. Недостаточное развитие желтого тела обусловливает низкую продукцию прогестерона в период лютеиновой фазы, тогда как продукция эстрогена остается полноценной, что нарушает равновесие между возбуждающим и тормозным влиянием этих гормонов на нервную систему (см. рис. 2). Таким образом, к влиянию нейростероидов, приводящему к усилению предрасположенности к развитию приступов при катамениальной эпилепсии, относят: отсутствие перед менструацией антиконвульсантного эффекта нейростероидов, опосредованного путем их взаимодействия с ГАМКА-рецепторами; изменения субъединиц ГАМКА-рецепторов и последующие нарушения нейронального ингибирования; внезапный пик эстрогенов за день до овуляции; повышенная частота ановуляторных циклов вследствие нарушения регуляции гипоталамо-гипофизарно-гонадной оси и, как следствие, прогестероновой недостаточности в лютеиновую фазу. Согласно последней усовершенствованной модели катамениальной эпилепсии (использовали мышей женского пола с киндлингом (Киндлинг (англ. Kindling – зажигание, возгорание) – стойкое изменение функционального состояния (возбудимости) отдельных зон головного мозга, возникающее в результате их постоянной подпороговой стумуляции) гиппокампа) первые два из этих механизмов являются основными в развитии катамениальных приступов: недостаток прогестерона перед менструацией в сочетании с невосприимчивостью ГАМКА-рецепторов к нейростероидам вследствие измененного строения субъединицы в менструальную фазу (предменструальную у женщин) привел к усилению приступов.
Хотя термин «катамениальная эпилепсия» не указывает на тип приступов, локализацию или эпилептический синдром, чаще всего катамениальный паттерн наблюдается при фокальной эпилепсии. Предположительная заболеваемость катамениальной эпилепсией широко варьирует в зависимости от диагностических критериев, которые используют исследователи. Например, если катамениальную эпилепсию определять в случаях, когда 75% приступов приходится на промежуток между 24-м днем одного цикла и 6-м днем следующего, то ее можно диагностировать приблизительно у 12,5% женщин с эпилепсией. Однако, когда Herzog et al. статистически выделили паттерны развития приступов в период менструального цикла, было выявлено последовательное удвоение частоты приступов в течение трех определенных частей менструального цикла (рамка 2), и приблизительно одну треть женщин с фокальной эпилепсией включили в группу с катамениальными приступами. Описание паттернов приступов представлено в рамке 2, а биологическое обоснование с учетом колебаний гормонов в течение менструального цикла — на рис. 2.
|
Перименструальный паттерн Перименструальный паттерн (С1) определяется как максимальная частота приступов в фазу менструации (период с 25-го дня одного цикла до 3-го дня следующего), которая коррелирует с недостатком прогестерона и является одним из наиболее часто встречаемых паттернов Периовуляторный паттерн Периовуляторный паттерн (С2) является вторым по распространенности паттерном, характеризуется максимальной частотой приступов в период овуляторной фазы (10-15-й день) и коррелирует с резким повышением концентрации эстрогена Лютеиновый паттерн Лютеиновый паттерн (СЗ) характеризуется максимальной частотой приступов в период овуляции, середине лютеиновой фазы и в менструальной фазе (10-й день одного цикла — 3-й день следующего цикла) по сравнению с частотой в середине фолликулярной фазы (3-10-й день) у женщин с недостаточностью лютеиновой фазы цикла; это третий, наиболее часто встречающийся паттерн, который коррелирует с низкой концентрацией прогестерона, обнаруженной при ановуляторных циклах |
Наличие трех превалирующих паттернов катамениальных приступов — перименструального (С1), периовуляторного (С2) и лютеинового (СЗ) — было подтверждено в многочисленных исследованиях. В одном из сообщений описаны паттерны катамениальных приступов, коррелирующие с пониженным уровнем прогестерона. Напротив, результаты другого исследования указывали на изменения концентрации эстрогена в качестве индикатора катамениального паттерна с незначительными изменениями уровня прогестерона между изучаемыми группами. Результаты других исследований указывают на роль гормонов, которые участвуют в развитии у женщин с эпилепсией приступов и циклических паттернов приступов, в том числе описан риск развития приступов, привнесенный ановуляторными циклами. Таким образом, циклические колебания уровня как эстрогена, так и прогестерона связаны с паттернами развития приступов при катамениальной эпилепсии.
Помимо влияния нейростероидов на развитие катамениальных приступов также на протяжении менструального цикла могут наблюдаться колебания концентрации АЭП. Существует фармакокинетический механизм, который может потенциально связывать уровень гормонов на протяжении менструального цикла с концентрацией АЭП. Так, высокие показатели циркулирующего эстрогена в лютеиновую фазу могут индуцировать печеночные изоферменты, участвующие в метаболизме АЭП, и таким образом снижать концентрацию циркулирующих АЭП перед менструацией, что потенциально способствует обвалу приступов. Rosciszewska et al. сообщили, что у женщин с катамениальными приступами уровень фенитоина на 28-й день цикла был статистически значимо ниже, чем у женщин без циклических обострений. Однако концентрация фенобарбитала статистически значимо не изменялась. Тем не менее по результатам обследования женщин с катамениальной эпилепсией связь между уровнями эстрадиола и прогестерона и концентрацией АЭП в сыворотке крови отсутствовала. Авторы предположили, что обострение катамениальных приступов не зависит от концентрации АЭП и более тесно связано с прогнозируемыми циклическими колебаниями уровня гормонов. По результатам одного исследования установлено, что уровень ламотриджина оставался неизменным на протяжении менструального цикла, хотя в другом — сообщалось о его снижении на 31% в середине лютеиновой фазы, при этом уровень вальпроатов не изменялся на протяжении всего цикла. Таким образом, доказательства не свидетельствуют в поддержку того, что изменения концентрации АЭП вносят существенный вклад в обострение катамениальных приступов, но при этом достоверно установлено существование независимого влияния нейростероидов.
Проводилась оценка большинства вмешательств при изучении предменструального паттерна приступов (С1) (см. рамку 2) — наиболее частого типа катамениального обострения. Женщинам с регулярным менструальным циклом показаны такие вмешательства, поскольку лекарственные средства необходимо принимать в определенные дни после наступления менструального кровотечения (рис. 3). Лечение обычно начинают во второй половине цикла (14-26-й день) в зависимости от индивидуального паттерна приступов и продолжительности менструального цикла, помня о том, что лютеиновая фаза длится 14 дней.
 Алгоритм лечения катамениальных приступов при выявлении паттерна С1
Алгоритм лечения катамениальных приступов при выявлении паттерна С1
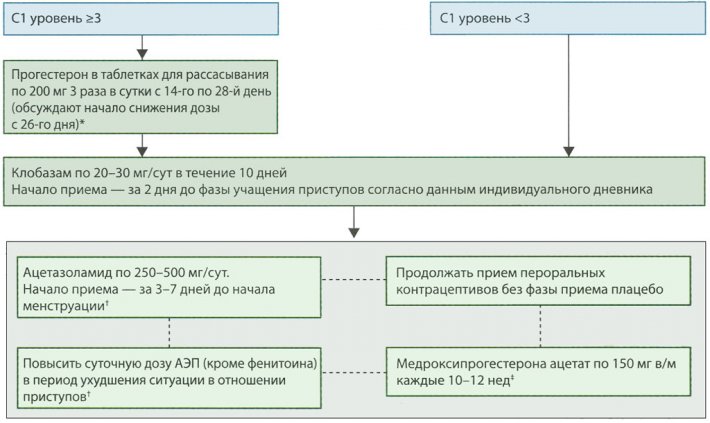
Рисунок 3. Алгоритм лечения катамениальных приступов при выявлении паттерна С1
Большинство существующих способов лечения применяются для лечения фокальных приступов у женщин с регулярной менструацией. С1 уровень 3 – повышение частоты приступов в три раза и более в период с 25-го дня одного цикла до 3-го дня следующего по сравнению с другими днями цикла.
АЭП – антиэпилептические препараты.
В/м – внутримышечно.
* - если менструация начинается с 26-го дня, начинают снижать дозу в этот же день в соответствии с такой же схемой снижения.
+ - метод широко применяется, но не подтвержден данными рандомизированных контролируемых испытаний.
++ - повышенный риск развития остеопороза и медленное возобновление нормальной фертильности.
Ацетазоламид используют для лечения катамениальной эпилепсии на протяжении 50 лет, хотя такое его применение не оценивали в ходе рандомизированных испытаний. Есть сообщения о его эффективности при назначении в дозе 250-500 мг/сут за 3-7 дней до начала менструации.
Бензодиазепины преимущественно используют для купирования кластеров приступов, но их назначают периодически из-за риска развития зависимости и резистентности при длительном применении. Клобазам является единственным препаратом группы бензодиазепинов, применение которого при катамениальной эпилепсии было официально изучено. По результатам двойного слепого, плацебо-контролируемого, перекрестного исследования прием клобазама был связан с лучшим контролем приступов по сравнению с плацебо. У большинства пациенток на протяжении 10-дневного лечения был достигнут полный контроль приступов.
Другой оправданный эмпирический подход заключается во временном повышении дозы АЭП, который обычно принимает пациентка во время определенных периодов на протяжении менструального цикла. При этом не следует повышать дозу фенитоина из-за риска токсического воздействия, связанного с нелинейной фармакокинетикой этого препарата.
Медроксипрогестерона ацетат представляет собой синтетическое вещество прогестинового ряда с контрацептивным действием. Его механизм действия в отношении снижения частоты приступов неизвестен, но предполагают, что он связан с блокированием циклических изменений уровня эстрогена и прогестерона. У пациентов с катамениальной эпилепсией применение медроксипрогестерона ацетата ассоциировалось со снижением частоты приступов на 39% при контрольном исследовании через один год. Медроксипрогестерона ацетат, введенный внутримышечно, останавливает регулярный менструальный цикл. Стандартная доза составляет 150 мг внутримышечно каждые 12 нед. Некоторые клиницисты выступают за укорочение интервала между вводимыми дозами до 10 нед в целях уменьшения риска снижения концентрации медроксипрогестерона ацетата под влиянием фермент-индуцирующих АЭП. Однако следует учитывать, что прием медроксипрогестерона ацетата, так же как и многих АЭП, связан с повышенным риском развития остеопороза. Кроме того, после прекращения введения медроксипрогестерона ацетата уровень эндогенных гормонов может значительно колебаться в течение нескольких месяцев, что чревато обострением приступов, а также может потребоваться длительное время для нормализации уровня фертильности. Некоторые клиницисты применяют стратегию подавления нормального циклического высвобождения гормонов репродуктивной системы при помощи непрерывного применения пероральных противозачаточных таблеток, которые подавляют овуляцию. Данные об эффективности такой стратегии, полученные в ходе контролируемых клинических испытаний, отсутствуют.
Превращение природного прогестерона в аллопрегнанолон, нейростероидный антиконвульсант, дает возможность контролировать приступы. По результатам двух небольших открытых исследований, в которых оценивали применение природного прогестерона в качестве лечебного средства при сложных парцильных приступах, при этом одно из исследований включало в себя долгосрочный период наблюдения, было высказано предположение, что применение природного прогестерона в форме вагинальных суппозиториев или таблеток для рассасывания с момента овуляции (14-й день) и до начала менструации является эффективным при лечении катамениальной эпилепсии. В ходе рандомизированного двойного слепого, плацебо-контролируемого, многоцентрового исследования было установлено, что степень перименструального обострения приступов (паттерн С1) являлась статистически значимым предиктором положительной ответной реакции на лечение прогестероном. При этом прогестерон назначали в форме таблеток для рассасывания (200 мг) 2 раза в сутки с 14-го по 28-й день цикла. Количество пациенток, положительно ответивших на лечение, не отличалось при приеме прогестерона или плацебо, когда всех участниц объединили, или между всеми пациентками с катамениальной эпилепсией по сравнению с некатамениальной. Тем не менее вторичный анализ показал, что уровень перименструального обострения приступов (паттерн С1) являлся предиктором положительной ответной реакции на прием прогестерона. Если у женщин наблюдалось увеличение количества приступов в три раза и более на протяжении периода С1 (плюс-минус 3 дня) по сравнению с другими днями цикла, то у 37,8% отмечался положительный ответ на лечение прогестероном (снижение частоты приступов на 50% и более; в группе плацебо — на 11,1%). У женщин, у которых в период С1 частота приступов повысилась в 8 раз и более, количество приступов сократилось примерно на 70%. При проведении наблюдения во время фазы открытого дополнительного лечения доза прогестерона у большинства женщин могла быть снижена до 100 мг 2 раза в сутки на 26-27-й день, до 50 мг 2 раза в сутки на 28-й день, а затем прием остановлен до 14-го дня следующего цикла. Если менструация начиналась до 26-го дня, то дозу снижали в этот день. К редким побочным эффектам природного прогестерона относят нагрубание молочных желез, утомляемость, депрессивное настроение и мажущие кровянистые выделения из влагалища.
Недостаточная в целом редукция частоты приступов согласно исследованию Herzog et al., за исключением пациенток со специфическими предменструальными приступами, указывает на то, что дополнительный прием прогестерона подавляет приступы, связанные с его недостатком, согласно молекулярным моделям и моделям in vivo. Однако эта гипотеза подразумевает невозможность эффективного лечения прогестероном женщин с катамениальными приступами, развивающимися в период овуляции. Следовательно, в случае совместного анализа данных о пациентках с различными паттернами катамениальных приступов (как в этом исследовании) общая польза от применения природного прогестерона может не выявляться. Дополнительным доказательством эффективности применения прогестерона у пациенток с паттерном С1 обострения приступов служит тот факт, что его польза возрастала по мере укорочения фазы приступов и их ограничения перименструальными днями.
В рамке 3 представлен алгоритм исследования и лечения пациенток с катамениальными приступами. В случае выявления катамениального паттерна С1 представлен алгоритм лечения (см. рис. 3).
|
Приведены рекомендации авторов в порядке обсуждения, основанного на клиническом опыте и ограниченном количестве доступных доказательств. 1. Обсуждение катамениального паттерна у женщин репродуктивного возраста с эпилепсией, которые не принимают какие-либо половые гормоны (например, пероральные контрацептивы) и у которых приступы продолжаются, несмотря на лечение традиционными АЭП. 2. Изучение дневников приступов, предпочтительно за период не менее трех менструальных циклов: а) для оценки связи между частотой приступов и началом менструации; б) для определения, если менструации регулярные (каждые 26-32 дня), проведения запланированных вмешательств. 3. Если менструация носит регулярный характер (см. рис. 3) и если приступы фокальные, обсуждается возможность лечения природным прогестероном: а) определить, имеется ли повышение частоты приступов в период С1 (от -3 до +3 дня) в три раза и более по сравнению с другими днями цикла; б) если таковое имеется, рассмотреть вопрос о лечении прогестероном: таблетки для рассасывания по 200 мг 3 раза в сутки с 14-го по 25-й день, а затем снижение до 100 мг 3 раза в сутки на 26-27-й день, по 50 мг три раза в сутки на 28-й день, затем прекращение приема (если менструация начинается до 26-го дня, снижение следует начинать в этот же день). 4. Если менструация носит регулярный характер (см. рис. 3) и паттерн катамениальных приступов соответствует паттерну С1, С2 или СЗ: а) рассмотреть вопрос о назначении клобазама по 20-30 мг каждый вечер в течение 10 дней с началом приема за 2 дня до периода, когда обычного развиваются приступы; б) рассмотреть вопрос о назначительном повышении дозы препарата, который обычно принимает пациентка, за 2 дня до периода, когда обычно развиваются приступы; 5. Если менструация носит нерегулярный характер: а) рассмотреть вопрос о подавлении менструального цикла при помощи пероральных контрацептивов, которые подавляют менструации в течение множества циклов, если не выявлено их значимого взаимодействия с принимаемыми АЭП (примечание: хотя этот подход применяется многими врачами-практиками, нет публикаций об исходах); б) если катамениальные обострения тяжелые и не поддаются лечению при помощи других вмешательств, рассмотреть вопрос о применении медроксипрогестерона ацетата при условии надлежащего обсуждения побочных эффектов. |
Синдром поликистозных яичников (СПКЯ) является основной причиной бесплодия и, по-видимому, чаще встречается у женщин с эпилепсией, чем в общей популяции. Что именно определяет развитие СПКЯ — остается целью исследования; по сообщению рабочей группы Общества по изучению избытка андрогенов и СПКЯ (Androgen Excess and PCOS Society) критерии СПКЯ определяются как наличие гиперандрогении (клинически и/или биохимически), дисфункции яичников (олигоановуляция и/или поликистоз яичников), а также при исключении родственных заболеваний. Предполагают, что СПКЯ является многофакторным заболеванием, чувствительным к различным экзогенным триггерам. Вероятно, при СПКЯ возникает нарушение гипоталамической и гипофизарной регуляции, о чем свидетельствует повышение секреции ЛГ и увеличение показателя соотношения ЛГ/ ФСГ. ФСГ стимулирует образование стероидов в яичниках, увеличение соотношения ЛГ/ФСГ будет приводить к продуцированию фолликулов, которые созрели не до конца, но при этом они многочисленны и кистозно изменены. В незрелых фолликулах наблюдается дефицит ароматазы, фермента, участвующего в синтезе эстрогена в яичниках из его предшественника тестостерона. Таким образом, фолликулы яичников при СПКЯ продуцируют преимущественно андрогены. Эта неправильная система повреждается дальше при трансформации андрогенов в эстрогены под воздействием ароматазы на периферии, повышая уровень циркулирующих эстрогенов, при этом по механизму обратной связи с гипофизом нарушается регуляция секреции ЛГ.
У женщин с эпилепсией гипоталамическая дисфункция может приводить к повышению частоты развития СПКЯ, а также к потере фолликулов яичниками и наступлению ранней менопаузы. Увеличение соотношения ЛГ/ФСГ было описано у женщин с локально- обусловленной эпилепсией и идиопатической генерализованной эпилепсией, при этом в последней группе этот показатель был самым высоким. Однако многие женщины с идиопатической генерализованной эпилепсией принимали вальпроаты, что могло исказить полученный результат.
Isojarvi et al. в 1993 г. впервые сообщили о наличии связи между приемом вальпроатов и кистозными изменениями яичников. Они сообщили, что приблизительно у половины из 13 женщин с эпилепсией, находящихся на монотерапии вальпроатами, были выявлены кисты яичников (без полностью развившегося СПКЯ), аменорея, олигоменорея или пролонгированный менструальный цикл по сравнению с 19% женщин, принимающих карбамазепин в качестве монотерапии. По результатам когортного исследования, проведенного этой же группой, было сообщено, что у 70% из 37 женщин с эпилепсией, принимавших вальпроаты, наблюдался поликистоз яичников и/или гиперандрогенизм по сравнению с 19% из 52 лиц группы контроля.
Также было установлено, что у женщин с эпилепсией при прекращении приема вальпроатов редуцировались признаки воздействия на обмен веществ — ожирение по центральному типу, гиперинсулинемия, нарушение липидного обмена, поликистоз яичников и гиперандрогенизм. Прием вальпроатов также может обусловливать развитие другого распространенного проявления СПКЯ — ожирения; результаты недавно проведенного исследования указывают на то, что вальпроаты подавляют обмен инсулина, что приводит к повышению уровня циркулирующего инсулина и, следовательно, к усилению резистентности к инсулину.
В ходе другого недавно выполненного исследования с участием 102 женщин репродуктивного возраста с эпилепсией СПКЯ был выявлен у 12% из них. Его диагностировали при наличии двух следующих составляющих и более: поликистоз яичников, гиперандрогенизм и аменорея или олигоменорея (а-/олигоменорея). У пациенток с СПКЯ дебют эпилепсии приходился в среднем на возраст 13,8 года (стандартное отклонение (SD) 6,5), заболевание развивалось статистически значимо раньше, чем у женщин без этих нарушений (16,9 (8,6) года; р<0,05). По данным этого исследования установлено, что терапия вальпроатами связана с повышенной частотой возникновения СПКЯ.
Показатели распространенности СПКЯ не полностью совпадают по данным литературы, вероятно, из-за определений, применяемых в исследованиях: если проводилась оценка составляющих СПКЯ, то результаты могут отличаться от полученных при оценке синдрома целиком. По результатам другого исследования, направленного на изучение только СПКЯ, не было выявлено различий в показателях у женщин, принимающих карбамазепин (10,0%), вальпроаты (11,1%) или вовсе не принимающих АЭП (10,5%). Эти показатели все-таки немного выше, чем показатель СПКЯ в общей популяции женщин, который составляет примерно 7%.
Все эти сообщения указывают на наличие прямой связи между эпилепсией и СПКЯ посредством гипоталамической дисфункции, а также на повышенный риск развития проявлений, совпадающих с СПКЯ, при применении вальпроатов. Возможно, эпилепсия сама по себе и прием вальпроатов являются двумя факторами риска развития СПКЯ.
Обследование женщин с эпилепсией должно включать в себя выявление нарушений менструального цикла, гирсутизма, акне, облысения по мужскому типу, а также измерение индекса массы тела. Следует проявлять настороженность по отношению к пациенткам, принимающим вальпроаты, и к женщинам с дебютом эпилепсии в молодом возрасте. У них простое скрининговое обследование должно включать определение уровня тестостерона и проспективное изучение длительности менструального цикла. Нормальная длительность менструального цикла, вероятно, коррелирует с наличием овуляции. В случае выявления признаков СПКЯ оправдано направление пациентки к эндокринологу и/или гинекологу для дальнейшего обследования и решения вопроса о вариантах лечения.
Применения вальпроатов следует избегать у женщин с детородным потенциалом в связи с высоким риском развития структурных тератогенных аномалий и пороков развития нервной системы. В таком случае необходимо обсуждать вопрос о назначении других АЭП. У мужчин с эпилепсией такие побочные эффекты, как увеличение массы тела и метаболический синдром, могут стать причиной постепенной или полной отмены терапии вальпроатами.
Во многих сообщениях говорится о физиологической сексуальной дисфункции у мужчин и женщин с эпилепсией. Однако роль фермент-индуцирующих АЭП, снижающих уровень андрогенов, неблагоприятное воздействие на настроение и существующие предрассудки в отношении сексуальности людей с эпилепсией свидетельствуют, что подходы к тактике ведения должны быть многоплановыми. Разумными стратегиями являются: определение уровня тестостерона с учетом влияния на него фермент-индуцирующих АЭП, выявление депрессии и тревожности, а также изучение социальных факторов.
О снижении показателей рождаемости сообщалось при изучении крупных когорт людей с эпилепсией. По результатам популяционного исследования обнаружено, что у мужчин с эпилепсией на 40% ниже показатель рождаемости, чем у мужчин без эпилепсии, а у женщин с эпилепсией он на 10% ниже, чем у женщин без эпилепсии. В более позднем исследовании при изучении той же популяции было выявлено, что у взрослых с активно протекающей эпилепсией снижены показатели рождаемости по сравнению с лицами, у которых ремиссия было достигнута еще до наступления зрелого возраста. Учитывая, что на показатели рождаемости влияет такой психосоциальный фактор, как сознательный отказ от рождения детей, показатель фертильности определяют у пар, не использующих методы контрацепции в течение одного года и не зачавших ребенка. Важное значение в обсуждении вопроса фертильности при эпилепсии на сегодня имеет Реестр эпилепсии и беременности штата Керала (Индия) (Kerala Registry of Epilepsy and Pregnancy). В этот реестр вносятся данные проспективного наблюдения молодых женщин с эпилепсией, которые после вступления в брак, как правило, пытаются забеременеть; бесплодие выявлено у 38% пациенток, что было связано с политерапией АЭП по сравнению с монотерапией. Обусловить снижение фертильности у женщин с эпилепсией могут несколько биологических причин, в том числе преждевременная недостаточность яичников, повышенный показатель ановуляторных циклов и частое развитие СПКЯ. Ановуляторные циклы встречаются у пациенток с эпилепсией чаще, чем у женщин группы контроля; согласно одному из сообщений после 3-месячного периода наблюдения было зарегистрировано, что частота ановуляторных циклов составляет 11% у лиц группы контроля, 14% — у пациенток с фокальной эпилепсией и 27% — у женщин с идиопатической генерализованной эпилепсией. У мужчин с эпилепсией нарушения сперматогенеза могут повышать риск бесплодия.
По результатам исследования с участием 60 мужчин с эпилепсией и 41 мужчины группы контроля частота выявления морфологически измененных сперматозоидов была статистически значимо выше среди пациентов с эпилепсией, получавших карбамазепин, окскарбазепин и вальпроаты, по сравнению с показателем у лиц группы контроля. Прием карбамазепина и вальпроатов был связан с плохой подвижностью сперматозоидов, а у принимавших карбамазепин часто наблюдалась патологически низкая концентрация сперматозоидов. У мужчин, принимавших вальпроаты и имеющих аномалии сперматозоидов, было выявлено уменьшение объема яичек, что согласуется с результатами лабораторных исследований, проведенных Sveberg Roste et al.. Согласно этому сообщению окскарбазепин в целом оказывал наименьшее неблагоприятное влияние. Другие исследователи сообщают о более высоких показателях нарушения подвижности сперматозоидов и морфологических аномалий сперматозоидов у мужчин с эпилепсией по сравнению с показателями у лиц группы контроля, что было связано с применением АЭП, в том числе вальпроатов и карбамазепина, а также фенитоина. Однако в работе Bauer et al. было высказано предположение о независимом неблагоприятном воздействии височной эпилепсии как таковой. Исследователи задокументировали недостаточность тестикулярной функции у мужчин, не принимающих АЭП, при этом прием фермент-индуцирующих АЭП оказывал дополнительное неблагорриятное влияние.
Не оценивались показатели рождаемости с поправкой на факторы, способные принципиально повлиять на результаты исследования (такие как частота половых актов или личный выбор иметь или не иметь детей), и которые имеют большое значение для людей с эпилепсией. Как уже было отмечено, к бесплодию могут приводить несколько биологических факторов, такие как нарушения менструального цикла у женщин вследствие нарушения центральной регуляции менструации, а также состояния, входящие в структуру СПКЯ. Существуют доказательства того, что политерапия АЭП вносит свой вклад в развитие бесплодия у женщин, и применение фермент-индуцирующих АЭП неблагоприятно влияет на качество спермы у мужчин.
Не существует четких стратегий по предотвращению бесплодия у больных с эпилепсией. Однако, если зачатие (при ведении половой жизни без контрацепции) не наступает течение 6 мес, то необходимо рассмотреть факторы, связанные с эпилепсией, в том числе прием АЭП.
У женщин следует провести оценку менструального цикла в целях определения частоты овуляторных циклов, наличия СПКЯ или раннего наступления перименопаузы (см. ниже).
У мужчин целесообразно выполнить анализ спермы и рассмотреть вопрос о замене АЭП, если результаты окажутся достоверно патологическими, особенно в случае применения фенитоина, карбамазепина или вальпроатов.
У женщин с эпилепсией существует риск раннего наступления менопаузы. Данный механизм, во всей вероятности, связан с дисфункцией гипоталамо-гипофизарно-гонадной оси, приводящей к нарушению регуляции созревания фолликулов яичника и преждевременной потере фолликулов, способных к овуляции. Одно из первых научных сообщений о ранней перименопаузе предоставили Klein et al., согласно которому у 14% пациенток с эпилепсией была выявлена преждевременная недостаточность яичников по сравнению с 4% у здоровых женщин группы контроля (р=0,04). Кроме того, у женщин с преждевременной недостаточностью яичников была выше вероятность катамениального обострения приступов ранее, в период репродуктивного возраста. Риск развития более ранней менопаузы, по-видимому, был связан с частотой приступов. Harden et al. сообщили о наличии отрицательной связи между возрастом на момент менопаузы и частотой приступов (р=0,014). Например, у женщин с редкими приступами возраст наступления менопаузы был в пределах нормы (50-51 год), тогда как у женщин с частыми приступами менопауза наступала раньше (в 46-47 лет). В этом исследованиии не было выявлено связи между ранним наступлением менопаузы и применением определенных АЭП.
Несмотря на отсутствие результатов проспективных исследований в отношении течения эпилепсии у женщин в период наступления менопаузы, доступны данные поперечного исследования с использованием почтового анкетирования, в котором женщин просили вспомнить, каким было течение эпилепсии в репродуктивный, перименопаузальный и менопаузальный периоды. Почти две трети женщин, находящихся в период перименопаузы, сообщили о повышении частоты приступов; указания в анамнезе на наличие паттерна катамениальных приступов было статистически значимо связано с возрастанием частоты приступов в перименопаузу. Эти результаты согласуются с возможными механизмами, характерными для женщин с гормонально-чувствительными приступами; в период перименопаузы уровень эстрогена остается неизменным, может неуклонно повышаться или стать неустойчивым с волнообразными скачками до начала менопаузы в ответ на повышенные уровня ФСГ. Однако циклическое повышение уровня прогестерона в лютеиновую фазу менструального цикла постепенно становится менее частым на протяжении перименопаузы, при этом увеличивается количество ановуляторных циклов. Увеличение отношения эстрогена к прогестерону может приводить к учащению приступов в период перименопаузы. Указание в анамнезе на наличие паттерна катамениальных приступов (приступы в течение недели, предшествующей менструации) было связано со снижением частоты приступов в период менопаузы. Большинству женщин в группе перименопаузы проводили заместительную терапию синтетическими гормонами, что было статистически значимо связано с увеличением количества приступов (р=0,001).
По результатам рандомизированного двойного слепого, плацебо-контролируемого испытания приема препарата Prempro (0,625 мг конъюгированных лошадиных эстрогенов плюс 2,5 мг медроксипрогесте- рона ацетата (CEE/MPA — conjugated equine oestrogens/ medroxyprogesterone acetate, Wyeth, Collegeville, штат Пенсильвания, США) однократно или двукратно в сутки в течение 3 мес установлено, что частота приступов статистически значимо возросла при применении Prempro по механизму дозозависимости. Полученные результаты демонстрируют неблагоприятное влияние экзогенных репродуктивных гормонов на женщин с эпилепсией в период менопаузы.
У пациенток с эпилепсией необходимо проявлять особую бдительность в отношении развития приступов в период перименопаузы, особенно если у них наблюдались паттерны катамениальных приступов. Им не показано назначение СЕЕ/МРА в качестве заместительной гормональной терапии в постменопаузальный период и, вероятно, следует рассмотреть другие схемы, такие как прием эстрадиола и природного прогестерона.
В области эпилепсии и нейроэндокринологии определены многие аспекты, и, что немаловажно, изучены действие нейростероидов на возбудимость головного мозга, реципрокные фармакокинетические взаимодействия, в том числе между эндогенными и экзогенными гормонами и АЭП, а также дезинтегрирующее действие на эндокринную систему эпилепсии как таковой. Клиницисты могут использовать эту информацию в качестве инструмента для совершенствования вариантов лечения мужчин и женщин с эпилепсией, например, преимущественно назначать АЭП с нейтральным гормональным действием и применять определенные стратегии лечения катамениальной эпилепсии.
Приоритеты исследований в этой области должны и дальше включать в себя изучение методов лечения катамениальной эпилепсии; результаты лучшего испытания, выполненного в настоящий момент, в котором использовалась гормональная терапия (природный прогестерон) для лечения подверженного влиянию гормонов паттерна приступов, являются многообещающими, но имеют свои ограничения. Популяция, в которой применение природного прогестерона, по-видимому, эффективно, очень специфическая и включает пациенток с обострением приступов в предменструальный период. Такой результат хорошо согласуется с нейро-стероидной теорией о дополнительном введении прогестерона в период предменструальной недостаточности прогестерона, но далек от комплексного решения проблемы связанных с менструальным циклом приступов у женщин. Учитывая нейрофизиологическую сложность эстрогена, прогестерона и тестостерона, необходимо провести исследования по применению гормональной стабилизирующей терапии у женщин с эпилепсией, предполагающей использование контрацептивов в стабильной дозе.
Другие направления исследования определяют и характеризуют влияние различных форм эпилепсии на репродуктивную функцию. Значение этих фактов может выходить за пределы репродуктивной области, может быть связано с влиянием на когнитивные возможности, а также аффективные и тревожные состояния у больных с эпилепсией. Влияние длительного приема АЭП более нового поколения на состояние репродуктивной системы остается неизвестным.
Результаты последних клинических исследований, получивших широкое признание, будут влиять на осознание того, что катамениальная эпилепсия потенциально излечима, а это в свою очередь повысит эффективность разработки практических подходов к лечению. К настоящему времени вальпроаты следует рассматривать как мощный дезинтегратор работы эндокринной системы, и при возможности искать альтернативы их применению. Современные и продолжающиеся исследования в дальнейшем будут предоставлять характеристики рисков бесплодия у людей с эпилепсией, что окажет помощь при осуществлении планирования семьи.
В скором будущем пациенты с эпилепсией получат пользу от лучшего понимания этих вопросов и готовности к применению специалистами современных знаний.
Перименопауза, или предклимактерический период, - это период репродуктивной жизни женщины,...
Геморрагическая трансформация ишемического инфаркта представляет собой область инфаркта...
Гормоны влияют на такое множество процессов в организме женщины, что практически каждое...
В давние времена специалисты предполагали, что для успешного оплодотворения необходимо...
Проблема гиперандрогении у женщин имеет несколько уровней реализации. Нарушение регуляции в...
анализы, БАД, биологическая медицина, витамины, гастроэнтерология, гигиена, гинекология, гомеопатия, дерматология, диагностика, диетология, заболевания, иммунология, инфекционные заболевания, инфекция, исследования, кардиология, кожа, косметика, красота, лекарственные растения, лечение, лицо, неврология, обследование, оздоровление, онкология, ортопедия, педиатрия, питание, пищеварительная система, поведение, похудение, препараты, продукты, профилактика, процедура, психология, пульмонология, рак, реабилитация, сердечно-сосудистая система, ССС, тело, терапия, травматология, уход, фитотерапия, хирургия, эндокринология
Показать все теги

Комменатрии к новости