Анемия при раке
Злокачественные патологии часто сопровождаются анемией – это форма анемии при...
Медицина / Патология / Патология (статья)
 АнемияХроническая болезнь почек (ХБП) подразумевает наличие любых маркеров повреждения почек, персистирующих на протяжение более трех месяцев, вне зависимости от патологии. Сам термин «хроническая болезнь почек» появился на рубеже XX и XXI вв вместо ранее использующегося термина «хроническая почечная недостаточность».
АнемияХроническая болезнь почек (ХБП) подразумевает наличие любых маркеров повреждения почек, персистирующих на протяжение более трех месяцев, вне зависимости от патологии. Сам термин «хроническая болезнь почек» появился на рубеже XX и XXI вв вместо ранее использующегося термина «хроническая почечная недостаточность».
Современная классификация ХБП основывается на двух главных показателях – признаки повреждения почек (альбуминурия, протеинурия) и скорости клубочковой фильтрации (СКФ) (см статью «Скорость клубочковой фильтрации (СКФ)»). В зависимости от сочетания этих показателей определяют одну из пяти стадий хронической болезни почек (таблица 1).
|
Стадия |
Описание |
Скорость клубочковой фильтрации (СКФ), |
|
I |
Признаки нефропатии, нормальная СКФ |
> 90 |
|
II |
Признаки нефропатии, незначительно снижение СКФ |
60-89 |
|
IIIA |
Умеренное снижение СКФ |
45-59 |
|
IIIБ |
Выраженное снижение СКФ |
30-44 |
|
IV |
Значительное снижение СКФ |
15-29 |
|
V |
Терминальная хроническая почечная недостаточность |
< 15 |
III-V стадии хронической болезни почек, при которых скорость клубочковой фильтрации снижается < 60 мл/мин), соответствуют определению «хроническая почечная недостаточность». V стадия – уремия – соответствует терминальной почечной недостаточности.
Сама концепция хронической болезни почек объединяет разные по этиологии и патогенезу заболевания, характеризующихся двумя основными факторами:
Хроническая болезнь почек сопровождается разными гематологическими проявлениями: аномалии тромбоцитов и свертывания крови, нарушения функции лейкоцитов, а также анемия.
Отметим, что анемия – наиболее видимое и характерное проявление хронической болезни почек, которое считается частным случаем анемии хронических заболеваний (АХЗ). Английский врач Ричард Брайт (Richard Bright) первый стал отмечать у больных с патологией почек бледность кожных покровов. С тех пор многие специалисты пытались объяснить и охарактеризовать механизмы нефрогенной анемии.
Степень тяжести анемии только приблизительно соответствует степени тяжести уремии – точной линейной корреляции между этими параметрами нет. Однако, если содержание азота мочевины в крови превышает показатель 36 ммоль/л, уровень гематокрита, как правило, всегда ниже 30%.
При хронической болезни почек патогенез анемии очень сложный, главным фактором которого, несомненно, является абсолютный или относительный дефицит эндогенного эритропоэтина (ЭПО). При развитии нефрогенной анемии, помимо недостаточной эндокринной функции почек и дефицита эритропоэтина относительно потребностей организма в эритроцитах, в основе патогенеза лежат факторы, связанные с развивающимся уремическим дисметаболизмом и нарушениями экскреторной функции почек. Уровень эритропоэтина у больных с разными стадиями хронической болезни почек гораздо ниже, чем у больных с анемией и нормальной функцией почек.
У пациентов с хронической болезнью почек не существует известного обратного соотношения между уровнем гемоглобина (гематокрита) и уровнем эритропоэтина, которое характерно у больных с анемией и нормальной функцией почек. У детей с ХБП уровень эндогенного эритропоэтина на определенной стадии был выше положенного диапазона, однако этот уровень представлял неадекватную реакцию на степень анемии по сравнению с реакцией ЭПО у детей с анемией и нормальной функцией почек.
Взаимосвязь между патологией почек и секрецией эритропоэтина нельзя описать в виде простой модели. Теоретически повреждения почек может влиять на образование эритропоэтина следующими путями:
Тот факт, что эритропоэтин-продуцирующий аппарат поврежденной почки может начать вырабатывать чрезмерное количество ЭПО после трансплантации почки (это явление наблюдается при посттрансплантационном эритроцитозе), свидетельствует о возможности обратимости функционального повреждения эритропоэтин-продуцирующих клеток при патологиях почек.
Клинические наблюдения показывают, что недостаточное образование эритропоэтина в почках (абсолютное или относительное) – главный фактор развития нефрогенной анемии. Также одним из факторов развития анемии при хронической болезни почек является гемолитический фактор – гемолиз, - наличие которого усугубляет степень тяжести нефрогенной анемии (в этом случае гипопролиферативный костный мозг не способен компенсировать потерю эритроцитов путем повышения их продукции).
Примерно у 1/3-1/2 всех больных хронической болезнью почек наблюдаются кровоподтеки и кровотечения в желудочно-кишечном тракте, а также маточные кровотечения. Кроме этого, во время диализа также происходят кровопотери (такие пациенты ежедневно теряют около 5-6 мг железа, или примерно 2 г железа в год). Такие кровопотери требуют усиления эритропоэза и способствуют в значительной степени развитию анемии. Нефрогенная анемия часто сопровождается дефицитом витамина B9 (фолиевой кислоты) и железа (дефицит железа может возникать из-за рецидивирующих кровотечений желудочно-кишечного тракта или маточными кровотечениями). Большое значение имеют резидуальные кровопотери при гемодиализе и неоправданно большое количество анализов крови. Дефицит фолиевой кислоты и железа при хронической болезни почек вызывает депрессию эритропоэза и образование неполноценных эритроцитов с коротким периодом жизни, что также может быть дополнительным фактором гемолитического состояния.
Анемия при хронической почечной недостаточности (ХПН), как правило, нормохромная и нормоцитарная. Количество ретикулоцитов может быть снижено, нормальное или незначительно повышенное и может повышаться при гипоксии или гемолизе. Степень тяжести анемии вариабельна (для нефрогенной анемии характерны колебания уровня гемоглобина в диапазоне 55-120 г/л; гематокрита – 17-35%). При микроскопическом исследовании на окрашенных мазках крови обнаруживаются деформированные эритроциты с большим количеством крошечных шипов, резко измененными (ненормальными) контурами и уменьшенным объемом (см рисунок 1).
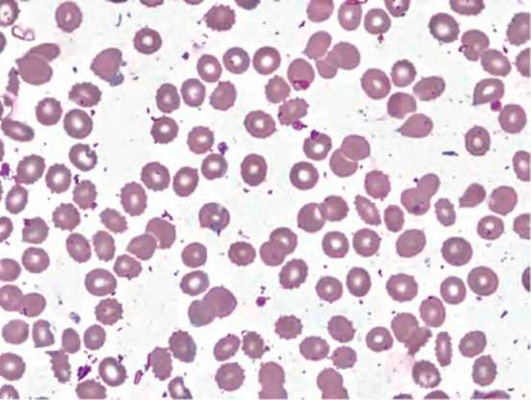
Рисунок 1. Анемия при хронической почечной недостаточности. Периферическая кровь. Эхиноциты (окр. по Романовскому-Гимзе, ув. ×100)
В некоторых случаях костный мозг может обнаруживать уменьшение клеточности, а в случае острой почечной недостаточности наблюдается тяжелая эритроидная гипоплазия. При хронической почечной недостаточности уровень ферритина в крови, как правило, повышен. По мнению специалистов, показатель уровня ферритина при ХПН ниже значений 40-105 мкг/л говорит о дефиците железа. В большинстве случаев патология, которая привела к развитию почечной недостаточности, приводит к специфическим изменениям кинетики железа и его содержания, фолиевой кислоты и трансферрина в крови. такие изменения способны повышать относительную недостаточность костного мозга, характерную для нефрогенной анемии.
Kidney Disease: Improving Global Outcomes (KDIGO) в 2012 году опубликовали клинические рекомендации, в которых авторы представили данные обобщенного опыта лечения анемии при хронической болезни почек эритропоэз-стимулирующими агентами (ЭСА), препаратами железа и другими лекарственными средствами. Также специалисты предоставили обоснованные рекомендации по диагностике анемии при хронической болезни почек.
Так, диагноз «анемия» при хронической болезни почек ставится у взрослых и детей старше 15 лет, если уровень гемоглобина (Hb) < 130 г/л у мужчин и < 120 г/л у женщин. У детей с ХБП в возрасте от 6 месяцев до 5 лет диагноз «анемия» ставится при уровне гемоглобина < 110 г/л; от 5 до 12 лет – Hb < 115 г/л; от 12 до 15 лет – Hb < 120 г/л. Пациентам с хронической болезнью почек, у которых не обнаружена анемия, рекомендуется проводить анализ крови на содержание гемоглобина при следующих показаниях:
Пациентам с анемией при ХБН, которые не получают ЭСА-терапию, анализ на содержание гемоглобина необходимо проводить при следующих показаниях:
При хронической болезни почек возникает дефицит железа из-за капиллярных кровотечений и резидуальных кровопотерь на мембранах диализатора и при лабораторных исследованиях. Определение уровня ферритина в крови считается наиболее ценным анализом для определения запасов железа. Уровень ферритина < 30 мкг/л свидетельствует о дефиците железа и дает основания для назначения препаратов железа. Отметим, что таким пациентам препараты железа рекомендуется вводить парентерально.
В рекомендациях KDIGO (2012 год) предлагается больным с анемией при ХБН, которые не получают лечение железосодержащими препаратами или ЭСА-терапию, назначать пробное лечение препаратами железа путем внутривенного введения (пациентам на додиализных стадиях хронической болезни почек – 1-3-месячный курс перорального приема препаратов железа).
Больным с ХБП, которые получают ЭСА-терапию и не получают препараты железа, рекомендуется назначить пробную терапию препаратами железа путем внутривенного введения (пациентам на додиализных стадиях хронической болезни почек – 1-3-месячный курс перорального приема препаратов железа), если необходимо повысить уровень гемоглобина или снизить дозировку ЭСА-препарата, гематокрит (степень насыщения трансферрина железом) < 30% и ферритин < 500 нг/мл (мкг/л).
Пациентам с ХБН на додиализной стадии, нуждающимся в терапии препаратами железа, выбор способа введения препарата необходимо основывать с учетом следующих моментов:
Дальнейшие назначения препаратов железа должны проводиться с учетом ответа на изменение уровня гемоглобина на проведенную ранее терапию, наличия продолжающихся потерь железа, результатов анализов на запасы железа (гематокрит, степень насыщения трансферрином, ферритин), настоящего уровня гемоглобина, ответа на ЭСА-терапию (в том числе на дозировки ЭСА-препарата), а также отмечать текущие изменения этих показателей и клинического состояния больного. Так как все препараты железа для внутривенного введения способны вызывать серьезные побочные эффекты, их нужно применять очень осторожно.
Сегодня наиболее популярный и эффективный способ лечения нефрогенной анемии – ЭСА-терапия как на додиализном этапе, так и во время заместительной почечной терапии (гемодиализа или перитонеального диализа).
До момента клинического применения ЭСА-терапии лечение анемии у пациентов на диализе было паллиативным: гемотрансфузии, ликвидация железодефицита и нехватки фолиевой кислоты. Несомненно, некоторым больным с тяжелой формной нефрогенной анемии необходима гемотрансфузия. Тем не менее, в наше время лечение анемии путем регулярного проведения гемотрансфузии проводится очень редко (гемотрансфузию назначают в тех случаях, когда риск побочных эффектов от ЭСА превышает ожидаемый лечебный эффект у пациентов, анамнез которых содержит инсульт, злокачественные патологии и др). В большинстве случаев анемия при хронической болезни почек лечится эритропоэз-стимулирующими агентами.
Препараты эритропоэтина – неотъемлемая часть комплексного лечения пациентов с терминальной уремией. Назначение эритропоэтина позволяет избежать проведения регулярных гемотрансфузий (без назначения ЭСА-терапии гемотрансфузии проводят 2-3 раза в месяц по 1000 мл каждая), а также связанных с ними рисками заражения инфекционными заболеваниями (гепатит, ВИЧ и др) и возникновения трансфузионных реакций. Также нужно отметить, что донорская кровь, введенная пациенту с ХПН, быстро секвестрируется, а изменение уровня гемоглобина носит волнообразный характер с выраженными пиками концентрации. Назначение ЭСА-терапии позволяет поддерживать стабильный уровень гемоглобина в крови, что улучшает состояние пациентов.
Очень важно исключить другие причины развития анемии:
Перед назначением ЭСА-терапии перечисленные выше состояния должны быть скорригированы. Если любые другие причины развития анемии отсутствуют (больной страдает только ХБН), пациенты с уровнем гемоглобина < 80 г/л почти всегда получат благоприятный ответ на ЭСА-терапию. При уровне гемоглобина 80-100 г/л и анемическом синдроме (см статью «Анемия. Общие положения. Классификация»), в том числе и стенокардии, пациенту показана ЭСА-терапия. Помимо уровня гемоглобина (или показателя гематокрита) неадекватно низкий уровень эритропоэтина в крови относительно степени анемии считается одним из основных критериев назначения ЭСА-терапии.
Эритропоэз-стимулирующие агенты (ЭСА) – эффективные современные средства коррекции анемии у больных хронической болезнью почек. Наиболее популярный ЭСА-препарат – Эральфон (альфа-эпоэтин; аналоги: Бинокрит, Гемакс, Эмавейл). Назначение дозы альфа-эпоэтина зависит от индивидуальных особенностей конкретного пациента, поэтому на фармакологическом рынке представлена довольно широкая линейка доз препарата, что является преимуществом при его назначении, особенно на этапе подбора дозировки (препарат реализуется в дозировках 1000 МЕ, 2000 МЕ, 2500 МЕ, 3000 МЕ, 4000 МЕ, 5000 МЕ, 10 000 МЕ, 20 000 МЕ, 40 000 МЕ). Таким образом врач может легко подобрать необходимую схему лечения в зависимости от массы тела больного, исходного уровня гемоглобина, а также выбрать наиболее удобную кратность введения препарата.
Отметим, что для ряда пациентов с хронической болезнью почек принципиально важно снизить кратность парентерального введения препарата и сохранить постоянную стимуляцию эритропоэза. Этого можно достичь путем применения пролонгированных форм ЭСА-препаратов – Дарбэпоэтин-альфа (Аранесп). Пролонгированные формы эритропоэз-стимулирующих агентов позволяют достигать стабильного гемопоэтического эффекта при режиме введения 1 раз в 2-4 недели (это особенно важно у пациентов с хронической болезнью почек III-IV стадии, а также у больных, находящихся на перитонеальном диализе).
Эпоэтин тета (Эпоратио) при подкожном введении назначается в начальной дозировке 20 МЕ/кг 3 раза в неделю. Если при этом уровень гемоглобина недостаточно повышается (менее 0,62 ммоль/л (1 г/дл) на протяжение 4 недель), дозу препарата повышают до 40 МЕ/кг 3 раза в неделю каждые 4 недели. В случае необходимости дозу Эпоэтин тета можно дополнительно увеличивать на 25% от предыдущей дозы с интервалом 1 месяц до момента индивидуального целевого уровня гемоглобина. При внутривенном введении препарата начальная дозировка – 40 МЕ/кг 3 раза в неделю. Дополнительное повышение дозировки препарата до 80 МЕ/кг 3 раза в неделю назначают через 4 недели. По мере необходимости дозировку можно повышать на 25% от предыдущей дозы с интервалом 1 месяц. Отметим, что максимальная дозировка Эпоэтин тета – 700 МЕ/нед.
ЭСА-терапия, как правило, проводится в два этапа:
Эпоэтин бета (Веро-Эпоэтин, Рекормон, Эритростим) принято назначать в дозировке 100-200 МЕ/кг в неделю (общую дозировку делят на 2-3 дозы) для больных на гемодиализе. Практическое использование Эпоэтин бета 100 МЕ/кг в/в в конце диализа показало, что пик концентрации эритропоэтина в крови у пациентов достигал 1000-2000 мМЕ/мл, после чего, в течение 1,5-2 суток, уровень гормона быстро снижался с Т1/2 (период полувыведения) от 5 до 8 часов. Несмотря на рекомендации, в которых введение Эпоэтин бета показано вводить пациенту в течение последних 5 минут гемодиализа, некоторые специалисты вводят препарат в начале процедуры (исследования показали, что Эпоэтин бета не диализируется).
Средняя дозировка эритропоэз-стимулирующих агентов для поддержания уровня гематокрита в пределах 33-36% - 75 МЕ/кг в/в 3 раза в неделю. Некоторым больным назначались препараты в дозе более 150 МЕ/кг в/в 3 раза в неделю. Такую вариабельность дозировки препаратов при достижении целевого уровня гематокрита (или гемоглобина) можно объяснить десятикратным изменением уровней динамической устойчивости баланса эритропоэтина в крови при любой конкретной степени анемии у больных с ХПН.
Учитывая вышесказанное, наиболее рациональный подход к подбору начальной дозировки препарата – ступенчатое повышение дозы эритропоэз-стимулирующего агента с 75-100 МЕ/кг в/в 3 р/нед. Эта дозировка должна корректироваться каждые 2-6 недель, при условии устойчивого повышения гематокрита, но не выше чем на 1-2% в неделю. В случае повышения показателя гематокрита превышает 2% в неделю, дозу ЭСА необходимо снизить на 25%. И наоборот – при отсутствии ответной реакции на препарат, дозировку рекомендуется повысить на 25%. Не рекомендуется менять дозировку препарата чаще чем 1 раз в 4 недели, поскольку нельзя достоверно оценить эффективность ЭСА за более короткий срок. Целевой уровень гемоглобина (или гематокрита), как правило, достигается к 10-12-й неделе ЭСА-терапии пациентов на диализе.
У больных на перитонеальном диализе в одном из двух наиболее часто применяемых вариантов (постоянный циклический перитонеальный диализ или постоянный амбулаторный перитонеальный анализ) сохраняется более высокий показатель гематокрита, чем у больных, находящихся на постоянном поддерживающем гемодиализе. Таким образом, пациентам на перитонеальном диализе необходимость в проведении ЭСА-терапии не настолько критична, хотя и рекомендована. Разница между пациентами групп перитонеального диализа и гемодиализа вероятнее всего в том, что больные на постоянном амбулаторном перитонеальном диализе не подвержены постоянным резидуальным кровопотерям. У больных на перитонеальном диализе обнаруживается такая же ответная эритропоэтическая реакция на ЭСА-терапию и такие же позитивные эффекты, как у больных на гемодиализе.
Отметим, что начальная дозировка ЭСА у больных на перитонеальном диализе значительно ниже, чем при гемодиализе; а способ введения препарата – подкожно. Одна из серий клинических исследований предполагала подкожное введение ЭСА 2 раза в неделю на протяжении 12 месяцев. Начальная доза – 25 или 50 МЕ/кг. Коррекция дозировки проводилась 1 раз в 4 недели до достижения целевого уровня гемоглобина – 100-120 г/л. Средняя недельная доза в этих исследованиях была 105 МЕ/кг. Применяемая схема ЭСА-терапии позволила достичь целевого показателя уровня гемоглобина в среднем через 11,7 недель.
Также нужно обратить внимание на тот факт, что подкожный способ введения эритропоэз-стимулирующих агентов многие специалисты до настоящего времени считали более предпочтительным, в сравнении с внутривенным введением, не только при перитонеальным диализе, но и при гемодиализе. Но сегодня вопрос о преимуществах подкожного введения перед внутривенным способом введения препарата подвергся серьезному пересмотру, так как у некоторых диализных пациентов, получавших ЭСА-терапию на протяжение долгого времени, внезапно возникала парциальная красноклеточная аплазия (аутоиммунная гемолитическая анемия), вызванная чрезмерным образованием анти-ЭПО-антител. Опосредованная антителами парциальная красноклеточная аплазия имеет две основные отличительные особенности:
В рекомендациях KDIGO указано, что после постанови диагноза «парциальная красноклеточная аплазия, опосредованная антителами» необходимо сразу прекратить ЭСА-терапию. Исчезновению антител способствует иммуносупрессивная терапия. Проведенные ретроспективные исследования, в которых приняли участие 37 человек, перенесших парциальную красноклеточную аплазию при ЭСА-терапии (преимущественно Эпоэтин альфа), показали, что у 29 пациентов (78%), получавших иммуносупрессивную терапию, состояние улучшилось (выздоровление), в то время как остальные 8 больных, не получавших иммуносупрессивную терапию, не выздоровели. Возобновление ЭСА-терапии способно вызвать повторное увеличение антител. Отметим, что сегодня есть данные, которые отмечают успешную терапию парциальной красноклеточной аплазии с применением Пегинесатида (Омонтис) – синтетический пептидный антагонист рецепторов к эритропоэтину, использование которого в некоторых случаях позволяет избежать иммуносупрессивную терапию.
Учитывая тот факт, что у каждого пациента индивидуальная потребность организма в кислороде (особенно если брать во внимание возраст и степень физической активности), не существует единого мнения в вопросе оптимального уровня гемоглобина и гематокрита. Наиболее распространенным целевым уровнем гемоглобина считается 100-115 г/л, гематокрита – 30-33%. При таких показателях отношение риска возможных побочных эффектов к терапевтической цели наиболее минимальны. Несомненно, это не является аксиомой, поэтому необходимо брать во внимание состояние больного и назначать терапию в зависимости от индивидуальных особенностей пациента.
Ряд пациентов отмечают более лучшее качество жизни при большем уровне гемоглобина. Несмотря на это таких пациентов нужно информировать о вероятных рисках и потенциальных опасностях более высокого уровня гемоглобина.
Большинство специалистов категорически против назначения ЭСА-терапии, если уровень гемоглобина превышает показатель 130 г/л. Так как основная цель ЭСА-терапии – коррекция симптомов анемии (см статью «Анемия. Общие положения. Классификация»), - разные пороги, при которых происходит коррекция, могут влиять на соответствующий уровень гемоглобина. Рациональная скорость повышения уровня гемоглобина для большинства больных – 10 г/л в месяц.
При хронической болезни почек III-IV стадии с симптомами анемии также отмечался благоприятный эффект от ЭСА-терапии без каких-либо побочных действий на функции почек. Несколько проведенных исследований показали, что назначение эритропоэз-стимулирующих агентов больным ХБП III-IV стадии позволило увеличить уровень гемоглобина и показатель гематокрита, а также повысить толерантность к физическим нагрузкам, улучшить качество жизни и общее самочувствие. Как и у пациентов с терминальной стадией почечной недостаточности, у больных ХБП III-IV необходимо учитывать наличие других факторов (кроме хронической болезни почек), которые могут стать причиной или аггравацией анемии и ингибировать реакцию на ЭСА-терапию:
Кроме этого, нужно брать во внимание возможный антиэритропоэтиновый эффект широко применяемых в наши дни антигипертензивных препаратов (блокаторы рецепторов ангиотензина и ингибиторов ангиотензинпревращающего эффекта).
Перед назначением терапии эритропоэз-стимулирующими агентами необходимо провести минимальных набор лабораторных анализов:
Также нужно контролировать состояние объема внеклеточной жидкости и артериального давления.
Стартовая доза ЭСА, как правило, является 20-50 МЕ/кг 3 раза в неделю. Если показатель гематокрита, уровень гемоглобина или количество ретикулоцитов не повышаются в течение 4 недель с момента начала терапии, дозу препарата нужно увеличивать с интервалом 4 недели до тех пор, пока не будет достигнут целевой показатель гематокрита или гемоглобина.
Дарбэпоэтин-альфа (Аранесп) принято назначать, начиная с дозировки 0,45 мкг/кг 1 раз в неделю внутривенно или подкожно; или 0,75 мкг/кг массы тела 1 раз в 2 недели подкожно. Если уровень гемоглобина повышается более чем на 10 г/л в течение 2 недель, дозировка ЭСА-препарата необходимо снизить на 25%. При этом нецелесообразно полностью отказывать от ЭСА-терапии, так как отмена часто сопровождается резким снижением уровня гемоглобина ниже целевого показателя.
Больные ХБП III-IV стадии нуждаются в клиническом и лабораторном мониторинге в начальном периоде индукции и периоде назначения поддерживающей терапии. Помимо контроля уровня гемоглобина и гематокрита еженедельно надо контролировать состояние жидкости в организме и артериальное давление; 1 раз в 2-3 недели – количество ретикулоцитов; 1 раз в 3-6 недель – уровень азота, креатинина, мочевины, ферритина и электролитов в крови. Если показатель гематокрита превышает значение 35%, дозировка ЭСА должны быть снижена, а в случае превышения значения 40; ЭСА-терапию необходимо приостановить до снижения показателя гематокрита ниже 38%, после чего возобновить введение ЭСА в дозировке примерно 2/3-3/4 от предыдущей дозировки. При достижении поддерживающей дозы эритропоэз-стимулирующего агента, позволяющей удерживать показатель гематокрита в пределах 30-35% (дозировка может быть 25-200 МЕ/кг), лабораторные анализы следует проводить 1 раз в 4-6 недель.
Самый распространенный побочный эффект лечения эритропоэз-стимулирующими агентами – повышение артериального давления. Примерно у 23% больных с момента начала приема ЭСА наблюдается развитие или усугубление артериальной гипертензии. На протяжении долгого времени специалисты считали, что этот побочный эффект возникает из-за повышения уровня гемоглобина и эритроцитов с превышением целевого гематокрита и развития гипервискозного синдрома (сгущения крови). Но сегодня ученые выяснили, что, помимо уже известных факторов, существует и альтернативный механизм развития артериальной гипертензии, вызываемый непосредственным действием эритропоэз-стимулирующих агентов на стенки кровеносных сосудов, а также устранением гипоксической NO-зависимой вазодилатации и стремительным повышением общего периферического сосудистого сопротивления. В большинстве случаев, при использовании ЭСА развитие артериальной гипертензии успешно купируют путем адекватной ультрафильтрации или медикаментозна (путем назначения ингибиторов ангиотензинпревращающего агента, β-блокаторов, кальциевых блокаторов). Но, несмотря на эффективность указанных средств, нужно снизить дозировку (при необходимости, даже отменить) ЭСА или применить подкожный способ введения препарата (если до этого его вводили внутривенно).
Злокачественные патологии часто сопровождаются анемией – это форма анемии при...
Анемия хронических заболеваний занимает второе место среди всех видов анемий, после...
Скорость клубочковой фильтрации в нефрологии является параметром первостепенной важности,...
Определение уровня креатинина и мочевины в плазме или сыворотке крови часто включают в...
Анемия развивается в результате снижения количество гемоглобина и эритроцитов в крови. У детей...
анализы, БАД, биологическая медицина, витамины, гастроэнтерология, гигиена, гинекология, гомеопатия, дерматология, диагностика, диетология, заболевания, иммунология, инфекционные заболевания, инфекция, исследования, кардиология, кожа, косметика, красота, лекарственные растения, лечение, неврология, неонатология, обследование, оздоровление, онкология, ортопедия, педиатрия, питание, пищеварительная система, поведение, похудение, препараты, продукты, профилактика, процедура, психология, пульмонология, рак, реабилитация, сердечно-сосудистая система, ССС, тело, терапия, травматология, уход, фитотерапия, хирургия, эндокринология
Показать все теги

Комменатрии к новости